 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.教学能力
B.科研能力
C.创造力
D.终身学习
 更多“()使教师职业超越了单一的工匠式技能特征,并成为衡量教师专业化程度的核心指标。”相关的问题
更多“()使教师职业超越了单一的工匠式技能特征,并成为衡量教师专业化程度的核心指标。”相关的问题
第1题
第2题
N2O4(g)的分解反应为N2O4(g)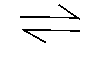 2NO2(g),在25℃时,Kθ,试求此温度下,当体系的平衡总压为200kPa时,N2O4(g)的平衡转化率。
2NO2(g),在25℃时,Kθ,试求此温度下,当体系的平衡总压为200kPa时,N2O4(g)的平衡转化率。
第3题
在308K和总压100kPa时,N2O4有27.2%分解为NO2。
(1)计算N2O4(g)==2NO2(g)反应的Kp;
(2)计算308K和总压2.026×105Pa时,N2O4的解离百分率;
(3)从计算结果说明压力对平衡移动的影响。
第4题
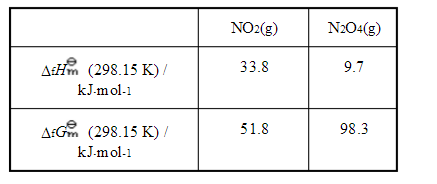
已知反应2NO2(g)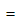 N2O4(g)及下表热力学数据,试计算该反应在298.15K和1000K时标准平衡常数
N2O4(g)及下表热力学数据,试计算该反应在298.15K和1000K时标准平衡常数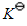 。
。
第5题
298 K时,反应N2O4(g)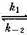 2NO2(g)的速率常数
2NO2(g)的速率常数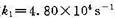 ,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为
,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为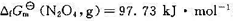 和
和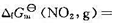 51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
第6题
若 298K 时反应N2O4 (g) = 2NO2(g) 的 Kө =0.1132,则当 N2O4 和 NO2 的分压均为1.0 kPa 时, 该反应()
A向生成 NO2 的方向进行
B向生成 N2O4 的方向进行
C正好达到化学平衡
D难于判断其进行方向
第7题
在1.013×105Pa下测得N2O4(g)在60℃时有50%离解,计算反应N2O4(g) 2NO2(g)的Kp。
2NO2(g)的Kp。
第8题

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
