 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.8.91×10-8
B.1.12×10-12
C.9.97×10-12
D.4.46×10-12
 更多“已知二元弱酸H2B溶液的浓度为0.5mol•L-1,Ka2=1.12×10-12H2B的Ka1=8.91×10-8,求B2-是()”相关的问题
更多“已知二元弱酸H2B溶液的浓度为0.5mol•L-1,Ka2=1.12×10-12H2B的Ka1=8.91×10-8,求B2-是()”相关的问题
第1题
A.[H+]=2c mol/L
B.[B2-]=c mol/L
C.[H2B]=c mol/L
D.[H2B]+[HB-]+[B2-]=c mol/L
第3题
A.2.0×10-10
B.5.0×10-14
C.3.2×10-8
D.2.0×10-16
第4题
用0.100mol•L-1的NaOH溶液滴定0.100mol•L-1二元弱酸H2B。已知:pH=0.74时,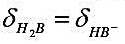 ;pH==6.50时,
;pH==6.50时,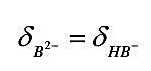 ;求该二元弱酸H2B的Ka1与Ka2。
;求该二元弱酸H2B的Ka1与Ka2。
第5题
第6题
二元弱酸H2B,已知pH=1.92时,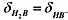 pH=6.22时,
pH=6.22时,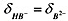 .
.
(1)计算H2B的Ka1和Ka2.
(2)若用0.100mol·L-1NaOH溶液滴定0.100mol·L-1H2B,滴定至第一和第二化学计量点时,溶液的pH各为多少?各选用何种指示剂?
第7题
二元弱酸H2B,已知pH=1.92时,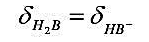 pH=6.22时,
pH=6.22时,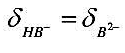 。
。
a.计算H2B的Ka1和Ka2;
b.若用0.1000mol•L-1NaOH溶液滴定0.1000mol•L-1H2B,滴定至第一和第二化学计量点时,溶液的pH各为多少?各选用何种指示剂?
第8题
用0.100mol·L-1的NaOH溶液滴定0.100mol·L-1二元弱酸H2B.已知:pH=0.74时,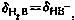 pH=6.50时,
pH=6.50时,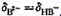 求该二元弱酸H2B的Ka1与Ka2.
求该二元弱酸H2B的Ka1与Ka2.
第9题
已知二元弱酸H2B的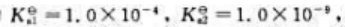 则二元弱碱B的K为().
则二元弱碱B的K为().
A、1.0×10-4
B、1.0×10-9
C、1.0×10-5
D、1.0×10-4
第10题
H2B为二元弱酸,pH=1.92时,δH2B=δHB-;pH=6.22时,δHB-=δB2-,计算(1)H2B的KA1和KA2;(2)当pH的值为多少时,二元弱酸以HB-的形式存在;(3)用0.100mol/L NaOH溶液滴定0.100mol/L H2B,滴定至第一和第二化学计量点时,溶液的pH值为多少?各选何种指示剂?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
