 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
过程单位时间最大反应量的计算
在循环流动固定床反应器中,若催化剂床层体积为2m3,床层空隙率为0.4,若液体中反应混合物浓度为1kmol/m3,采用例题8-2所计算的传质系数,计算反应器中最大反应速率。又若气相反应,气体中反应混合物浓度为10-2kmol/m3,通过2m3的催化剂床层,反应器的最大反应速率又为多少?
 更多“过程单位时间最大反应量的计算 在循环流动固定床反应器中,若催化剂床层体积为2m3,床层空隙率为0.4,若液体”相关的问题
更多“过程单位时间最大反应量的计算 在循环流动固定床反应器中,若催化剂床层体积为2m3,床层空隙率为0.4,若液体”相关的问题
第1题
表面温度与表面浓度
在ZnO~Fe2O3催化剂上进行乙炔水合反应
2C2H2+3H2O→CH3COCH3+CO2+2H2
为一级反应,其速率方程为
(-rA)=kcA
式中 cA——乙炔浓度;
k——反应速率常数。
在催化剂颗粒直径为5mm的固定床反应器中进行反应,已知床层中某处的压力为0.10133MPa,气相主体温度为390℃,乙炔浓度为2.8%体积分率,试计算该处催化剂外表面温度和乙炔浓度。已知外扩散阻力可忽略不计。反应气体的流量G为880kg/(m2·h)反应热效应为
(-AH)=177820kJ/kmol(C2H2)
反应气体物性数据如下:
μ=2.35×10-5Pa·s λg=0.2135kJ/(h·m·℃)
cP=2.01kJ/(kg·℃),D=0.73cm2/s,ρ=0.9kg/m3
第2题
内扩散阻力存在下的表观反应速率常数k
一级不可逆反应于某温度T下,以反应器为基准的反应速率常数k=2s-1,催化剂是直径为5mm的球形颗粒,床层空隙率ε=0.4,若求得内表面利用率η2=0.672,试计算下列两种情况下的表观反应速率常数k:
(1)催化剂颗粒改为直径为3mm的球形颗粒,若ε不变;
(2)改变充填方法,使催化剂的空隙率为0.50(粒度不变)。
第3题
颗粒直径与内扩散
某一级不可逆气-固催化反应,其反应速率为
(-rA)=kcA=10-6mol/(s·cm3)
当cA=10-2mol/L,0.10133MPa,400℃时,若要求催化剂内扩散对总速率基本上不发生影响,问催化剂粒径如何改变。已知De=10-3cm2/s。
第4题
内部效率因子计算
在一直径为6mm的多孔球形催化剂上发生二级不可逆反应A→B。当没有扩散影响时,反应的动力学方程为
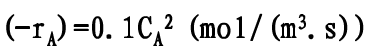 (mol/(m3·s))
(mol/(m3·s))
若A在气相中的浓度为100mol/m3,有效扩散系数为10-6m2/s,反应在恒温下进行,外扩散的影响可以忽略,试求催化剂的内部效率因子。
第5题
内扩散影响实验判别
在一固定床循环反应器中进行一级气相反应A→B。该反应器的循环比很高,因此在反应器内反应物的浓度是均匀的。在所有实验中进料速度均相同,υ0=3cm3/s,A的初始浓度cA0=100mol/m3,试根据下表中所列的实验数据确定内扩散对总反应过程起什么作用。
实验编号 | dP/cm | W/kg | xA |
1 | 0.2 | 2.0 | 0.6 |
2 | 0.6 | 1.0 | 0.2 |
第6题
内扩散影响程度实验研究
请考虑在一直径为1.8cm的球形催化剂颗粒上进行的一级反应A→P。实验数据列于下表:
T(℃) | cA(mol/m3) | R(mol/(m3·h)) |
13 | 100 | 270 |
30 | 5 | 100 |
72 | 1 | 400 |
97 | 0.1 | 110 |
127 | 0.01 | 30 |
上表中cA为A在气相的浓度。已知外扩散的阻力很小,可以忽略不计,因此cA也等于A在催化剂颗粒外表面上的浓度。
(1)试根据上述实验数据确定,温度在什么区域内扩散对总反应过程起控制作用。
(2)求反应的活化能。
第7题
颗粒内、外扩散影响的计算
用直径为6mm的球形催化剂进行一级不可逆反应A→P+R。气相主体中A的摩尔分率为yA=0.5,操作压力p=0.10133MPa,反应温度T=500℃,已知单位体积床层的反应速率常数为0.333s-1,床层空隙率为0.5,组分A在粒内有效扩散系数为0.00296cm2/s,外扩散传质系数为40m/h,试计算:
(1)催化剂内表面利用率η2,其影响是否严重?
(2)催化剂外表面浓度cA,es,并说明外扩散影响是否严重?
(3)计算表观反应速率。
第8题
颗粒内、外扩散影响的判断
用直径为1mm的球形颗粒进行一级不可逆反应A→P,气流主体中A的浓度为cA,b=0.01kmol/m3,测得单位床层表观反应速率R=400kmol/(m3·h),床层空隙率为0.4,组分A在粒内有效扩散系数为10-3m2/h,外部传质系数kg=50m/h。试计算内、外扩散对反应过程影响的程度。
第9题
颗粒内、外扩散影响实例分析
克宁汉(Cunningham)测定了CuO-MgO催化剂上乙烯加氢的总速率。使用的催化剂有两种形式:100目(颗粒直径为0.149mm)颗粒和三种密度的1.2mm球形颗粒。忽略两种形式表面浓度和温度差别。在100目颗粒和球形颗粒外表面上乙烯和氢几乎是同样浓度条件下的速率数据如下:
T(℃) | (-rA)×106 | R×106mol/(g(cat) ·s) | ||
100目颗粒(直径0.149mm) | 球形颗粒 | |||
ρP=0.72 | ρP=0.95 | ρP=1.18 | ||
124 | 14.5 | 6.8 | 4.3 | 2.2 |
112 | 6.8 | 6.7 | 4.2 | 2.1 |
97 | 2.9 | 6.4 | 4.0 | 2.0 |
84 | 1.2 | 6.0 | 3.7 | 1.9 |
72 | 5.5 | 3.4 | 1.7 | |
50 | 4.3 | 2.6 | 1.3 | |
问:
(1)确定反应过程的本征活化能;
(2)在所列出温度下计算每种密度球形颗粒的效率因子;
(3)为什么有的效率因子大于1,有些则小于1?
(4)为什么速率和效率因子随球形颗粒密度减小而增加?
第10题
颗粒的温度估算
在甲烷气-固催化氧化反应过程中,催化剂颗粒直径为6mm,试计算下列两种情况的颗粒中心与外表面间最大温差:
(1)反应气体中甲烷在空气中的浓度为0.02(摩尔分率);
(2)如果甲烷在空气中浓度提高到0.1(摩尔分率)。
假设外扩散阻力可忽略不计,并已知:
反应热效应
(-△H)=890360J/mol
颗粒内孔有效扩散系数为
De=0.00368cm2/s
颗粒的有效导热系数
λe=0.002218J/(s·cm·℃)
反应条件为0.10133MPa和450℃条件下等温反应。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
