 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“交通运输、建筑施工、危险化学品、烟花爆竹等行业或领域从事生产经营活动的企业风险抵押金存储标准,”相关的问题
更多“交通运输、建筑施工、危险化学品、烟花爆竹等行业或领域从事生产经营活动的企业风险抵押金存储标准,”相关的问题
第1题
pH=5.00时,以二甲酚橙为指示剂,用0.02000mol•L-1的EDTA溶液滴定0.02000mol•L-1的Zn2+溶液(其中含有0.020mol•L-1Ca2+),计算终点误差。已知pH=5.00时,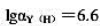 ,滴定终点的锌离子浓度
,滴定终点的锌离子浓度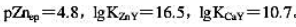 。
。
第2题
在pH=5.5时,以二甲酚橙作指示剂,用0.02000mol•L-1EDTA滴定0.020mol•L-1Zn2+和0.020mol•L-1Ca2+,计算化学计量点时的pZnsp和pCaY,并由计算说明能否准确滴定Zn2+。如果不能准确滴定,应采用何种措施,简述其理由。已知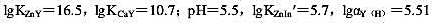 。
。
第3题
第4题
A.99.00%
B.80.70%
C.40.35%
D.8.07%
第5题
溶液中含有0.020mol•L-1的Th(Ⅳ)、La3+,用等浓度的EDTA溶液滴定,试设计以二甲酚橙作指示剂的测定方法。已知Th(OH)4的Ksp=10^-44.89,La(OH)3的Ksp=10^-18.8,二甲酚橙与La3+及Th(Ⅳ)的lgKMIn'如下:

第6题
在pH=10的氨性缓冲溶液中含有0.020mol·L-1Cu2+,若以PAN作指示剂,用0.020mol·L-1EDTA溶液滴定至终点,计算终点误差。(终点时,游离氨为0.10mol·L-1,pCuep=13.8。)
第7题
用0.020mol•L-1的EDTA滴定0.020mol•L-1的Zn2+离子,求△pM=0.2,Et=±0.3%时,滴定反应适宜的酸度范围。已知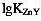 =16.5,
=16.5,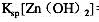 =10^-16.92,EDTA的
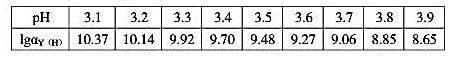
=10^-16.92,EDTA的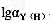 与pH之间的对应关系见下表。
与pH之间的对应关系见下表。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
