 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
pH=5.00时,以二甲酚橙为指示剂,用0.02000mol•L-1的EDTA溶液滴定0.02000mol•L-1的Zn2+溶液(其中含有0.020mol•L-1Ca2+),计算终点误差。已知pH=5.00时,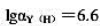 ,滴定终点的锌离子浓度
,滴定终点的锌离子浓度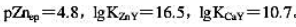 。
。
 更多“pH=5.00时,以二甲酚橙为指示剂,用0.02000mol•L-1的EDTA溶液滴定0.02000mol•L-1的Zn2+溶液(其中”相关的问题
更多“pH=5.00时,以二甲酚橙为指示剂,用0.02000mol•L-1的EDTA溶液滴定0.02000mol•L-1的Zn2+溶液(其中”相关的问题
第2题
向pH=5.0的20.00mL0.020mol?L-1Zn2+溶液中加入20.04mL0.0200mol?L-1EDTA溶液后,游离的[Y]和Zn2+各为多少?已知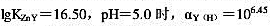 。
。
请帮忙给出正确答案和分析,谢谢!
第3题
测定锆英石中ZrO2、Fe2O3含量时,称取1.000g试样,以适当的熔样方法制成200.0mL试样溶液。移取50.00mL试液,调至pH=0.8,加入盐酸羟胺还原Fe3+,以二甲酚橙为指示剂,用1.000x10^-2mol?L-1EDTA溶液滴定,消耗10.00mL。加入浓硝酸,加热,使Fe2+被氧化为Fe3+,将溶液调至pH≈1.5,以磺基水杨酸作指示剂,用上述EDTA溶液滴定,消耗20.00mL。计算试样中ZrO2和Fe2O3的质量分数。
请帮忙给出正确答案和分析,谢谢!
第4题
用浓度为cEDTA=0.05000mol?L-1溶液滴定100.0mL浓度为cZn2+=0.0100mol?L-1的Zn2+,设滴定反应为: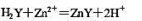 。滴定开始时,pH=5.50,若溶液中无缓冲溶液,滴定至终点时,溶液的pH为多少?通过计算说明EDTA配位滴定时加入缓冲溶液的必要性。
。滴定开始时,pH=5.50,若溶液中无缓冲溶液,滴定至终点时,溶液的pH为多少?通过计算说明EDTA配位滴定时加入缓冲溶液的必要性。
请帮忙给出正确答案和分析,谢谢!

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
