 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.P
B.Si
C.Cl
D.O
 更多“根据元素的电负性数值,判断下列原子中哪一个获得电子的能力最弱。”相关的问题
更多“根据元素的电负性数值,判断下列原子中哪一个获得电子的能力最弱。”相关的问题
第2题
不参看周期表,试推测下列每一对原子中哪一个原子具有较高的第一电离能和较大的电负性值?
(1) 19和29号元素原子; (2) 37和55号元素原子;(3) 37和38号元素原子。
第3题
第4题
不参看有关数据,试推测下列每一对原子中哪一个原子具有较高的第一电离能和较大的电负性? (1)19和29号元素; (2)37和55号元素; (3)37和38号元素
第5题
A.电负性用来描述不同元素的原子对键合电子吸引力的大小
B.电负性是以氟为4.0、锂为1.0作为标准的相对值
C.元素电负性越小,元素非金属性越强
D.元素电负性越大,元素非金属性越强
第6题
不用查表判断下列物质中中心原子元素电负性数值的大小和物质中化学键的极性由大到小的顺序:
H2O,H2S,H2Se,H2Te
第7题
比较下列各元素的性质:
(1)Si,S原子半径、电离能、电负性;
(2)Cl,Br原子半径、电离能、电负性;
(3)Nb,Ta原子半径。
第8题
A.主族元素的电负性越大,元素原子的第一电离能一定越大
B.在元素周期表中,元素电负性从左到右越来越小
C.金属元素的电负性一定小于非金属元素的电负性
D.在形成化合物时,电负性越小的元素越容易显正价
第9题
下表是某些短周期元素的电负性(用x表示)的数值:
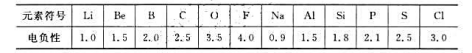
(1)通过分析上表中电负性的数值变化的规律,试确定Mg和N元素的电负性的数值范围() < x(Mg) < ()和() < x(N )< ()。
(2)同周期(同主族)元素的电负性与原子半径的关系是()。
(3)当形成化学键的两种元素的电负性的差值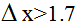 时,一般为离子键;当
时,一般为离子键;当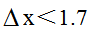 时,一般为共价键。则由此可知AlBr3中化学键的类型是()。
时,一般为共价键。则由此可知AlBr3中化学键的类型是()。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
