 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下表是某些短周期元素的电负性(用x表示)的数值:
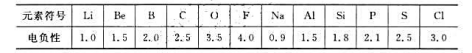
(1)通过分析上表中电负性的数值变化的规律,试确定Mg和N元素的电负性的数值范围() < x(Mg) < ()和() < x(N )< ()。
(2)同周期(同主族)元素的电负性与原子半径的关系是()。
(3)当形成化学键的两种元素的电负性的差值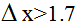 时,一般为离子键;当
时,一般为离子键;当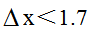 时,一般为共价键。则由此可知AlBr3中化学键的类型是()。
时,一般为共价键。则由此可知AlBr3中化学键的类型是()。
 更多“下表是某些短周期元素的电负性(用x表示)的数值: (1)通过分析上表中电负性的数值变化的规”相关的问题
更多“下表是某些短周期元素的电负性(用x表示)的数值: (1)通过分析上表中电负性的数值变化的规”相关的问题
第1题
第2题
现有部分短周期主族元素的描述如下表: 元素编号 元 素 描 述 W 人体内含量最多的元素,且其单质是常见的助燃剂 X 第三周期中半径最小的元素 Y 原子核外最外层电子排布为ns n np n Z 原子的最外层 p 亚层电子数等于次外层电子数 ()
第3题
A.X的原子半径大于Y的原子半径
B.X的电负性大于Y的电负性
C.X单质的氧化性小于Y单质的氧化性
D.X的第一电离能小于Y的第一电离能
第4题
A.含有X元素的化合物一定是共价化合物
B.Y元素的电负性大于X元素的电负性
C.X元素的单质与Z元素的单质在一定条件下能发生化合反应
D.W元素的单质能与NaOH溶液反应放出氢气
第5题
A.质子数:c>d,离子的还原性:Y2->Z-
B.电负性(指非金属性):Z>Y>W>X
C.原子半径:X
D.氢化物的稳定性:H2Y>HZ
第6题
A.y轴表示的可能是第一电离能
B.y轴表示的可能是电负性
C.y轴表示的可能是原子半径
D.y轴表示的可能是形成基态离子转移的电子数
第7题
A.R位于元素周期表中第二周期第ⅥA族
B.五种元素中原子半径最大的是X
C.气态氢化物稳定性:Y>T
D.Z元素的最高价氧化物对应水化物的化学式为HZO4
第9题
A.族③R元素第一电离能大于同周期相邻元素④R元素基态原子的电子排布式为1s22s2
B.②③
C.③④
D.①④

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
