 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
题目来源:1月6日下午江西省南昌市面试考题
试讲题目
1.题目:氦气的性质
2.内容:
氨是没有颜色、有刺激性气味的气体,极易溶解于水且溶解的快。在常温下,1体积的水大约可溶解700体积氨。氦的水溶液叫做氨水。氨溶于水时,大部分与水结合成一水合氨(NH3·H2O)。NH3·H2O很不稳定,受热就会分解为氨和水。
NH3+H2O═NH3·H2O
NH3·H2O═(△)NH3↑+H2O氨水有弱碱性,能使酚酞溶液变红或使红色石蕊试纸变蓝。
资料卡片
氨水为什么显碱性?
在常温下,一水合氨中有一小部分(约1%)电离或NH4+和OH-,所以氨水显弱碱性,能使酚酞溶液变红,按在水中的反应可以表示如下:
NH3+H20═NH3·H2O?NH4++OH-
NH3+H2O═NH4++OH-
氨与酸反应生成铵盐。如氨遇到氯化铵时,迅速反应生成氯化铵晶体。
NH3+HCl═NH4Cl
农业上常用的化肥,如硫酸铵、碳酸氢铵、硝酸铵等都是铵盐。铵盐都易溶于水,受热易分解,与碱反应时放出氨。
NH4Cl═NH3↑+HCI↑
NH4HCO3═(△)NH3↑+CO2↑+H2O
NH4NO3+NaOH═(△)NH3↑+NaNO3+H2O
前面介绍的工业上合成氨的反应是个可逆反应,这说明氨在同一条件下,能自动分解成N2和H2。氨还能被氧气氧化,生成一氧化碳,进而氧化成二氧化碳,用来制造硝酸。
3.基本要求:
(1)要求配合教学内容有简单的板书设计。
(2)教学过程中要有课堂互动环节。
(3)请在十分钟内完成试讲。
答辩题目
1.化学教师需要具备哪些实验教学的能力?
2.喷泉实验成功的关键有哪些?
 更多“题目来源:1月6日下午江西省南昌市面试考题试讲题目1.题目:氦气的性质2.内容:氨是没有颜色、有刺激”相关的问题
更多“题目来源:1月6日下午江西省南昌市面试考题试讲题目1.题目:氦气的性质2.内容:氨是没有颜色、有刺激”相关的问题
第1题
题目来源:1月6日下午山东省济南市面试考题
试讲题目
1.题目:Fe2+和Fe3+的转化
2.内容:
活动与探究
不同价态的铁的化合物在一定条件下能够相互转化,让我们
共同探究Fe2+和Fe3+的转化条件。
实验室提供下列试剂:铁粉、0.1mol·L-lFeCl3溶液、0.1mol·L-lFeCl2溶液、KSCN溶液、新制氯水。
1.请你根据氧化还原反应的基本原理,提出有关Fe2+和Fe3+相互转化条件的假设。
2.设计Fe2+和Fe3+相互转化的实验方案,进行实验并记录现象。
表3-5Fe2+和Fe3+的转化实验

3.用简洁的语言归纳Fe2+和Fe3+相互转化的条件。
3.基本要求:
(1)教学中注意师生间的交流互动,有适当的提问环节。
(2)如果需要实验或辅助教学工具,采用语言模拟即可。
(3)要求配合教学内容有适当的板书设计。
答辩题目
1.本节课主要应用了哪些教法和学法,目的是什么?
2.请问Fe2+转化为Fe3+的探究实验中需要注意什么?
第2题
题目来源:1月6日上午山东省临沂市面试考题
试讲题目
1.题目:原电池
2.内容:
要想使氧化还原反应释放的能量直接转变为电能,就要设计一种装置,使氧化反应和还原反应分别在两个不同的区域进行,并使其间的电子转移,在一定条件下形成电流。为了使用方便,还需要把可产生的电能以化学能的形式储存起来。化学电池就是这样一种装置。这种装置可以将氧化还原反应体系的能量储存起来,类似于水库的蓄存水能。
实验2-4
将锌片和铜片用导线连接(导线中间接入一个电流表),平行插入盛有稀硫酸的烧杯中(如图2-9),观察现象。

学与问
根据你所了解的电学知识,你知道电子是怎样流动的吗?你如何判定装置的正、负板?由于锌和铜的活动性不同,锌容易失去电子,被氧化成Zn2+进入溶液,电子由锌片通过导线流向铜片,溶液中的H+从铜片获得电子被还原成氢原子,氢原子再结合成氢分子从铜片上逸出。这一变化过程可以表示如下:
锌片:Zn-2e-=Zn2+(氧化反应)
铜片:2H++2e-=H2↑(还原反应)
我们把这种将化学能转为电能的装置叫做原电池,最早的化学电池就是根据原电池原理制成的。
3.基本要求:
(1)试讲过程中要设置互动环节。
(2)试讲要讲清原理与实验。
(3)试讲时要有适当的板书设计。
答辩题目
1.化学教学提问的基本要求是什么?
2.原电池反应时锌这端也会有气泡产生,是什么原因?怎样避免?
第3题
题目来源:1月6日上午河北省保定市面试考题
试讲题目
1.题目:乙醇
2.内容:
【观察与思考】
【实验1】观察钠的保存方法,并向1~2mL无水乙醇中投入一小粒金属钠,观察实验现象。
【实验2】向试管中加入3~4mL无水乙醇,浸入50℃左右的热水中,以保持反应所需温度。将铜丝烧热,迅速插入乙醇中,反复多次,观察并感受铜丝颜色和乙醇气味的变化。

思考下列问题:
1.实验1中金属钠与煤油、无水乙醇是否发生反应?从实验中你能得到什么启示?
2.在进行实验2的过程中,铜丝的颜色先后发生了什么变化?乙醇在实验中是被氧化还是被还原?
煤油是多种烷烃的混合物,实验表明这些烷烃分子中与碳原子相连的氢不能被金属钠置换。但乙醇分子中羟基(-OH)上的氢原子能被金属钠置换。我们已经知道水分子中-OH上的氢原子也能被金属钠置换,水与金属钠反应比乙醇与金属钠反应要剧烈得多。
金属钠与乙醇反应可用化学方程式表示为:
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
乙醇在铜、银等催化剂存在下可以被氧气氧化,生成具有特殊气味的乙醛。

3.基本要求:
(1)认识乙醇与钠的反应、乙醇的催化氧化反应。
(2)要求配合教学内容有适当板书设计。
(3)请在10分钟内完成试讲。
(4)教学过程中实验操作进行模拟演示即可。
答辩题目
1.你是如何导入新课的,为什么采用这种方法?
2.在醇生成烯烃的消去反应中,浓硫酸的作用是什么?
第4题
题目来源:1月6日上午黑龙江省大庆市面试考题
试讲题目
1.题目:物质的量
2.内容:
在研究物质转化的过程中,人们除了关注物质转化方法的选择、转化条件的控制以外,还十分关注转化过程中物质间的定量关系。
由于化学变化中涉及的原子、分子或离子等单个粒子的质量都很小,难以直接进行称量,而实际参加反应的粒子数目往往很大,为了将一定数目的微观粒子与可称量物质之间联系起来,在化学上特引入物质的量(amount of substance)。
物质的量是国际单位制中的基本物理量之一,符号为n,单位为摩尔(简称为摩,符号为mol)。1mol某种微粒集合体中所含的微粒数与0.012kgC-12中所含的原子数相同。0.012kgC-12中所含的原子数称为阿伏伽德罗常数。用NA表示。阿伏伽德罗常数NA近似为6.02×1023mol-1。例如:
1molO2中约含6.02×1023个氧分子;
1molC中约含6.02×1023个碳原子;
1molH2SO4中约含6.02×1023个硫酸分子;
1molNaOH中约含6.02×1023个Na+和6.02×1023个OH-;
nmol某种微粒集合体中所含微粒数约为n×6.02×1023。
物质的量(n)、阿伏伽德罗常数(NA)和微粒数(N)之间存在如下关系:
N=n×NA
3.基本要求:
(1)简要写出教学过程。
(2)教学过程中要有适当的提问环节。
(3)要求配合教学内容有适当板书设计。
(4)试讲时间十分钟。
答辩题目
1.提高课堂教学有效性的方法和策略是什么?
2.摩尔是物质的质量单位。这种说法对吗?
第5题
题目来源:1月6日上午湖南省长沙市面试考题
试讲题目
1.题目:钠的性质
2.内容:
金属钠(sodium)的化学性质很活泼,在化学反应中,钠原子很容易失去最外层的一个电子,形成钠离子
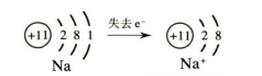
钠离子的形成
1.观察下列实验,并将观察到的现象及所得结论填入表2-3。
【实验1】取一小块金属钠,用滤纸吸干表面的煤油,用刀切去一端的表层,观察表面的颜色;将其放置在空气中,观察表面颜色的变化。
【实验2】将一小块金属钠放在石棉网上加热,观察实验现象。
【实验3】向一只盛有水的小烧杯中滴加几滴酚酞溶液,然后投入一小块(约绿豆粒般大小)金属钠,观察实验现象。
表2-3钠的性质实验
2.根据上述反应中钠元素化合价的变化情况,总结钠的性质。
观察与思考
钠是一种银白色金属,质软,密度为0.97g·cm-3,熔点为97.8℃。
钠单质能够与许多非金属单质、水等物质发生反应,反应中钠失去电子,表现出还原性。
2Na+H2O==2NaOH+H2↑
金属钠露置在空气中与氧气反应,生成白色的氧化钠;钠在空气中燃烧,生成淡黄色的过氧化钠。因此,实验室常将钠保存在煤油中。
4Na+O2==2Na2O
2Na+O2==(点燃)Na2O2
3.基本要求:
(1)让学生了解钠的物理化学性质,尤其是要掌握钠与水的反应。
(2)教学过程中若需要实验或者教具进行语言模拟演示即可。
(3)要求配合教学内容有适当板书设计。
(4)请在10分钟内完成试讲。
答辩题目
1.请你说明这堂课的设计思路?
2.如果金属钠燃烧,应该如何灭火?
第6题
题目来源:1月7日下午湖北省武汉市面试考题
试讲题目
1.题目:铁的冶炼
2.内容:
早在春秋战国时期,我国就开始生产和使用铁器,从公元1世纪起。铁便成了一种最主要的金属材料。
炼铁的原理是利川一氧化碳与氧钢化铁的反应。在实验室里,可以利用图8-20所示的装置进行实验。实验中玻璃管里的粉由红色逐渐变黑。这种黑色的粉未就是被还原出来的铁;试管里澄清的石灰水变浑浊。证明有二氧化碳生成。


氧化铁在加热时能被一氧化碳还原成铁,同时生成二氧化碳。
Fe2O3+3CO==(高温)2Fe+3CO2
铁矿石冶炼成铁是一个复杂的过程。把铁矿石和焦炭、石灰石一起加入高炉。在高温下,利用焦炭与氧气反成生成的一氧化碳把铁从铁矿石里还原出来。
在实际生产时,所用的原料或产物一般都含有杂质,在计算用科和产业时,应考虑到杂质问题。
3.基本要求:
(1)要有适当的板书设计。
(2)试讲10分钟以内。
(3)要有师生活动。
第7题
题目来源:1月7日下午广东省中山市面试考题
试讲题目
1.题目:置换反应
2.内容:
分析上述实验中镁、锌、铁与盐酸(或稀硫酸)的反应:
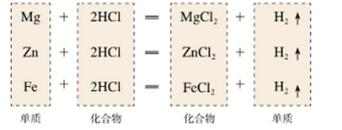
这几个反应都是由一种单质与一种化合物反应,生成另一种单质和另一种化合物。这种由一种单质与一种化合物反应,生成另一种单质和另一种化合物的反应叫做置换反应。
由上述探究可以得出,镁、锌、铁的金属活动性比铜的强,它们能置换出盐酸或稀硫酸中的氢
3.基本要求:
(1)要有适当的板书设计。
(2)试讲要条理清晰,重点突出。
(3)教学过程中注意对学生进行启发、引导。
第8题
题目来源:1月7日下午山东临沂面试考题
试讲题目
1.题目:空气的成分
2.内容:
实验2-1:
实验装置如图2-3所示,在集气瓶内加入少量水,并将水面上方空间分为5等份。用弹簧夹夹紧胶皮管。点燃燃烧匙内的红磷后,立即伸入瓶中并把塞子塞紧,观察红磷燃烧的现象。待红磷熄灭并冷却后,打开弹簧夹,观察实验现象及水面的变化情况。
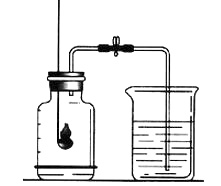
图2-3测定空气里氧气的含量
在这一反应中,红磷(化学符号P)与空气中的氧气反应,生成一种叫做五氧化二磷(化学符号P2O5)的新物质。这一反应可用文字表示如下:
红磷+氧气 五氧化二磷
五氧化二磷
集气瓶内水平面上升约1/5,说明空气中的氧气被消耗了,消耗的氧气约占空气体积的1/5。
在19世纪末以前,人们深信空气中仅含有氧气和氮气。后来人们陆续发现了氦、氖、氩、氪、氙、氡等稀有气体,才认识到空气中除了氧气和氮气外,还有其他成分。目前,人们已能用实验方法精确地测定空气的成分。
通过实验测定,空气的成分按体积计算,大约是:氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%。
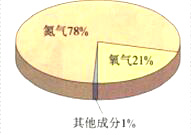
图2-4空气成分示意图
3.基本要求:
(1)要求配合教学内容有简单的板书设计。
(2)教学过程中要有课堂互动环节。
(3)请在十分钟内完成试讲。
第9题
题目来源:1月7日上午山东省淄博市面试考题
试讲题目
1.题目:溶液的配制
2.内容:明确任务
(1)与同学合作配制80g10%的氯化钠溶液
(2)初步学会配制一定溶质质量分数溶液的方法

做好准备
(1)你需要准备以下实验用品:托盘天平、烧杯、玻璃棒、钥匙、量筒(10mL、100mL);氯化钠、蒸馏水。
(2)你需要回顾托盘天平(或电子秤)的使用方法,以及量取和搅拌液体等操作方法。
友情提示
用玻璃棒搅拌液体时,要注意不要尽量使玻璃棒碰触容器的器壁。
动手实验

按上述步骤完成实验并将表格中各项内容补充完整。
3.基本要求:
(1)要有适当的板书设计。
(2)试讲要条理清晰,重点突出。
(3)教学过程中注意对学生进行启发、引导。
第10题
题目来源:1月7日上午天津面试考题
试讲题目
1.题目:利用化学方程式的简单计算
2.内容:
研究物质的化学变化。常要涉及量的计算,根据化学方程式的计算就可以从量的方面研究物质的变化。例如,用一定量的原料最多可以生产出多少产品?制备一定量的产品最少需要多少原料?等等。通过计算,可以加强生产的计划性,并有利于合理地利用资源。
下面,用实例来说明利用化学方程式进行计算的步骤和方法,
【例题1】加热分解6.3g高锰酸钾,可以得到氧气的质量是多少?(计算结果保留一位小数)
【解】设:加热分解63g高锰酸钾可以得到氧气的
(1)设未知量
(2)写出反应的化学方程式
(3)写出相关物质的化学计量数与相对分子质量的乘积以及已知量、未知量
(4)列出比例式,求解
(5)简明地写出答案

3.基本要求:
(1)要有适当的板书设计。
(2)试讲要条理清晰,重点突出。
(3)教学过程中注意对学生进行启发、引导。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
