 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.研和法
B.溶解法
C.熔合法
D.乳化法
E.分散法
 更多“软膏剂的制备方法A.研和法B.溶解法C.熔合法D.乳化法E.分散”相关的问题
更多“软膏剂的制备方法A.研和法B.溶解法C.熔合法D.乳化法E.分散”相关的问题
第1题
将下列反应设计为电池 (1)Zn+Cl4(p)→ZnCl2(aq) (2)Zn(s)+Hg2SO4(s)→ZnSO4(a)+2Hg(l) (3)AgCl(s)+
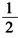 H2(p)→HCl(a)+Ag(s) (4)H2(p1)+
H2(p)→HCl(a)+Ag(s) (4)H2(p1)+
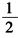 O4(p4)→H2O(l) (5)Ag2O2(s)+2H2O(1)+2Zn(s)→2Ag(s)+2Zn(OH)2(s) (6)I2(s)+I-(a1)一I3-(a2)
O4(p4)→H2O(l) (5)Ag2O2(s)+2H2O(1)+2Zn(s)→2Ag(s)+2Zn(OH)2(s) (6)I2(s)+I-(a1)一I3-(a2)
第2题
将下列反应设计成原电池: (1)H2 O(1)=OH-+H+ (2)Cl2+2Ag=2AgCI(s) (3)4NH3+Cu2+=[Cu(NH3)4]2+
第3题
如果将下列氧化还原反应装配成原电池,试用符号表示所组成的原电池。 (1)Zn(s)+2Ag+(aq)=Zn2+(aq)+2Ag(s) (2)Cu(s)+2FeCl3(aq)=CuCl2(aq)+2FeCl2(aq) (3)Sn2+(aq)+2Fe3+(aq)=Sn4+(aq)+2Fe2+(aq) (4)Zn(s)+2HCl(aq)=ZnCl2(aq)+H2(g) (5)MnO4-(0.1molL-1)+8H+(10-4 molL-1)+5Fe2+(0.1molL-1)=Mn2+(0.1 molL-1)+5Fe3+(0.1 molL-1)+4H2O(l)
第4题
将下列化学反应设计成电池:
(1)Zn+Cd2+(aCd2+)=-Zn2+(aZn2+)+Cd;
(2)Cl2(pCl2)+2I-(aI-)=I2(s)+2CI-(aC1-);
(3)Pb+2HCl(a)=PbCl2(s)+H2(pH2);
(4)(1/2)H2(pH2)+AgCl(s)=Ag+HCl(a);
(5)H2(pH2)+I2(s)=2HI(a).
第5题
由反应Fe(s)+2Ag+(aq)=Fe2+(aq)+2Ag(s)组成原电池,若仅将Ag+浓度减小到原来浓度的1/10,则电池电动势会()。
A.增大0.059V
B.减小0.059V
C.减小0.118V
D.增大0.118V
第6题
反应Zn(s)+2AgCl(s)===2Ag(s)+ZnCl2(aq)可以设计成原电池,其图式为______。
第7题
试写出下列各电池的电极反应和电池反应。 (1)Cu(s)|CuSO4(a1)||AgNO3(a2)|Ag(s) (2)Pb(s)|PbSO4(s)|K2SO4(a1)||HCl(a2)|AgCl(s)|Ag(s) (3)Pt|H2(P)|NaOH(a)|HgO(s)|Hg(1) (4)Pt|H2(P1)|H2SO4(m)|H2(P2)|Pt (5)K(Hg)(a1)|K+(a2)||Cl-(a3)|Hg2Cl2(s)|Hg(1)
第8题
写出下列浓差电池的电池反应,并计算298K时的电池电动势。 (1)Pt|H2(pΘ)|H+(a1=0.01)||H+(a2=0.1)|H2(pΘ)|Pt (2)Pt|Cl2(pΘ)|Cl-(a=1)|Cl2(2pΘ)|Pt (3)Ag(s)|AgCl(s)|Cl-(a1=0.01)||Cl-(a1=0.002)|AgCl(S)|Ag(s) (4)Cu(s)|Cu2+(a1=0.004)||Cu2+(a2=0.01)|Cu(s)
第9题
标准状态下,将下列反应设计成原电池。
(1)H++Zn→Zn2++H2
(2)Fe3++Hg+Cl-→Hg2Cl2+Fe2+
(3)Pb2++SO2-4→PbSO4
(4)Ag++2NH3→[Ag(NH3)2]+

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
