 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


电池Ag(s)|AgCl(s)|KCl(m)|Hg2Cl2(s)|Hg(l)的电池反应为 Ag(s)+
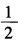 Hg2Cl2(s)→Agcl(s)+Hg(l) 已知298K时,此电池反应的焓变△rHm为5435J/mol,各物质的规定熵数据为 物质 Ag(s) AgCl(s) Hg(1) Hg2Cl2(s) SmΘ/(J/K.mol) 42.7 96.2 77.4 195.6 试计算该温度下电池的电动势E及电池电动势的温度系数
Hg2Cl2(s)→Agcl(s)+Hg(l) 已知298K时,此电池反应的焓变△rHm为5435J/mol,各物质的规定熵数据为 物质 Ag(s) AgCl(s) Hg(1) Hg2Cl2(s) SmΘ/(J/K.mol) 42.7 96.2 77.4 195.6 试计算该温度下电池的电动势E及电池电动势的温度系数
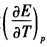 。
。
 更多“电池Ag(s)|AgCl(s)|KCl(m)|Hg2Cl2(s)|Hg(l)的电池反应为 Ag(s)+Hg2Cl2(s)→Agcl(s)+Hg(l)”相关的问题
更多“电池Ag(s)|AgCl(s)|KCl(m)|Hg2Cl2(s)|Hg(l)的电池反应为 Ag(s)+Hg2Cl2(s)→Agcl(s)+Hg(l)”相关的问题
第1题
用电解沉积的办法分离Cd2+和Zn2+,已知H2在Cd上的超电势为0.48V,在Zn上的超电势为0.70V,溶液中的Cd2+和Zn2+浓度皆为0.1 moL/kg。(已知
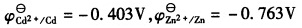 ,离子的活度系数均为1,溶液的pH保持中性。)通过计算回答下面的问题: (1)哪种金属首先在阴极上析出? (2)第二种金属开始析出时,前一种金属剩下的浓度为多少? (3)当H2开始析出时,溶液中残留的两种金属的浓度各为多少?
,离子的活度系数均为1,溶液的pH保持中性。)通过计算回答下面的问题: (1)哪种金属首先在阴极上析出? (2)第二种金属开始析出时,前一种金属剩下的浓度为多少? (3)当H2开始析出时,溶液中残留的两种金属的浓度各为多少?
请帮忙给出正确答案和分析,谢谢!
第2题
某溶液中NaCl的浓度为0.001moL/kg,Na2SO4的浓度为0.003mol/kg,试计算298K时该溶液的(1)离子强度;(2)各离子的活度系数;(3)各化合物的离子平均活度。
请帮忙给出正确答案和分析,谢谢!
第3题
将下列反应设计为电池 (1)Zn+Cl4(p)→ZnCl2(aq) (2)Zn(s)+Hg2SO4(s)→ZnSO4(a)+2Hg(l) (3)AgCl(s)+
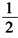 H2(p)→HCl(a)+Ag(s) (4)H2(p1)+
H2(p)→HCl(a)+Ag(s) (4)H2(p1)+
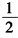 O4(p4)→H2O(l) (5)Ag2O2(s)+2H2O(1)+2Zn(s)→2Ag(s)+2Zn(OH)2(s) (6)I2(s)+I-(a1)一I3-(a2)
O4(p4)→H2O(l) (5)Ag2O2(s)+2H2O(1)+2Zn(s)→2Ag(s)+2Zn(OH)2(s) (6)I2(s)+I-(a1)一I3-(a2)
请帮忙给出正确答案和分析,谢谢!
第4题
现有电池zn(s)|ZnCl2(m)|AgCl(s)|Ag(s),在下面的空格内选择阴、阳,正、负填人。作为原电池时,Zn电极是_______极、_______极;作为电解池时,Zn电极是_______极、_______极。
请帮忙给出正确答案和分析,谢谢!

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
