 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
根据下列各逻辑式,画出逻辑图:
(1)Y=(A+B)C; (2)Y=AB+BC;
(3)Y=(A+B)(A+C); (4)Y=A+BC;
(5)Y=A(B+C)+BC。
 更多“根据下列各逻辑式,画出逻辑图: (1)Y=(AB)C; (2)Y=ABBC; (3)Y=(AB)(AC); (4)Y=ABC; (5)Y=A(BC)B”相关的问题
更多“根据下列各逻辑式,画出逻辑图: (1)Y=(AB)C; (2)Y=ABBC; (3)Y=(AB)(AC); (4)Y=ABC; (5)Y=A(BC)B”相关的问题
第1题
在101.325kPa下,HNO3、H2O系统的组成为:
| T/K | 373 | 383 | 393 | 395 | 393 | 388 | 383 | 373 | 358.5 |
| x(HNO3)液 y(HNO3)所 | 0.00 0.00 | 0.11 0.01 | 0.27 0.17 | 0.38 0.38 | 0.45 0.70 | 0.52 0.90 | 0.60 0.96 | 0.75 0.98 | 1.00 1.00 |

第2题
标准压力下,HNO3-H2O系统的组成为:

(1)画出此系统的t-x图;
(2)将3molHNO3和2molH2O的混合气冷却到114℃,互,相平衡的两相组成为何?互比量为若干?
(3)将3molHNO3利2molH2O的混合物蒸馏,待溶液沸点升高了4℃时,整个馏出物组成约为若干?
(4)将(3)中所给混合物进行完全燕馏,能得何物?
第3题
A,B二组分在液态完全互溶,已知液体B在80℃下蒸气压力为101.325kPa,汽化焓为30.76kJ·mol-1。组分A的正常沸点比组分B的正常沸点高10℃。在101.325kPa下将8mol的A和2mol的B混合加热到60℃产生第一个气泡,其组成为yB=0.4,继续在101.325kPa下等压封闭加热到70℃,剩下最后一滴液其组成为xB=0.1。将7mol的B和3mol的A气体混合,在101.325kPa下冷却到65℃产生第一滴液体,其组成为xB=0.9,继续等压封闭冷却到55℃时剩下最后一个气泡,其组成为yB=0.6。
(1)画出此二组分系统在101.325kPa下的沸点一组成图,并标出各相区;
(2)8molB和2molA的混合物在101.325kPa,65℃时,①求平衡气相的物质的量;②求平衡液相中组分B的活度和活度因子(系数);③此混合物能否用简单精馏的方法分离为纯A组分与纯B组分,为什么?
第4题
101.325kPa下水(A)-醋酸(B)系统的气-液平衡数据如下。
(1)画出气-液平衡的温度-组成图。
(2)从图上找出组成为xB=0.800的气相的泡点。
(3)从图上找出组成为yB=0.800的液相的露点。
(4)105.0°C时气-液平衡两相的组成是多少?
(5)9kg水与30kg醋酸组成的系统在105.0°C达到平衡时,气一液两相的质量各位多少?
第5题
A.4
B.3
C.2
D.1
第6题
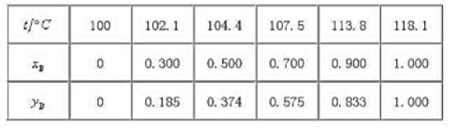
101.325kPa下水(A)-醋酸(B)系统的气-液平衡数据如表6-3所示。
表6-3 | ||||||
t/℃ | 100 | 102.1 | 104.4 | 107.5 | 113.8 | 118.1 |
xB | 0 | 0.300 | 0.500 | 0.700 | 0.900 | 1.000 |
yB | 0 | 0.185 | 0.374 | 0.575 | 0.833 | 1.000 |
(1)画出气-液平衡的温度-组成图;
(2)从图上找出组成为xB=0.800的液相的泡点;
(3)从图上找出组成为yB=0.800的气相的露点;
(4)105.0℃时气-液平衡两相的组成是多少?
(5)9kg水与30kg醋酸组成的系统在105.0℃达到平衡时,气、液两相的质量各为多少?
第7题
液体H2O(A),CCl4(B)的饱和蒸气压与温度的关系如表6-4所示。
表6-4
|
两液体成完全不互溶系统。
(1)绘出H2O-CCl4系统气、液、液三相平衡时气相中H2O,CCl4的蒸气分压对温度的关系曲线;
(2)从图中找出系统在外压101.325kPa下的共沸点;
(3)某组成为yB(含CCl4的摩尔分数)的H2O-CCl4气体混合物在101.325kPa下恒压冷却到80℃时,开始凝结出液体水,求此混合气体的组成;
(4)上述气体混合物继续冷却至70℃时,气相组成如何?
(5)上述气体混合物冷却到什么温度度时,CCl4也凝结成液体,此时气相组成如何?
第8题
水-异丁醇系统液相部分互溶。在101.325kPa下,系统的共沸点为89.7℃。气(G)、液(L1)、液(L2)三相平衡时的组成ω(异丁醇)依次为:70.0%,8.7%,85.0%。今由350g水和150g异丁醇形成的系统在101.325kPa压力下由室温加热,问:(1)温度刚要达到共沸点时,系统处于相平衡时存在哪些相?其质量各为多少?(2)当温度由共沸点刚有上升趋势时,系统处于相平衡时存在哪些相?其质量各为多少?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
