 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
设输入符号集与输出符号集为X=Y={0,1,2,3},且输入信源的分布为
P(X=i)=1/4,i=1,2,3,4
设失真矩阵为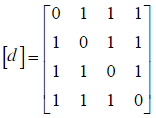 ,求Dmax、Dmin及R(D)。
,求Dmax、Dmin及R(D)。
 更多“3.设输入符号集与输出符号集为X=Y={0,1,2,3},且输入信源的分布为 P(X=i)=1/4,i=1,2,3,4 设失真矩阵为,求D”相关的问题
更多“3.设输入符号集与输出符号集为X=Y={0,1,2,3},且输入信源的分布为 P(X=i)=1/4,i=1,2,3,4 设失真矩阵为,求D”相关的问题
第1题
下列电池的电动势为0.981V。Zn|Zn2+(5.0×10-3mol/L),NH3(0.12mol/L) SHE计算下述反应的平衡常数K(25℃时)。
SHE计算下述反应的平衡常数K(25℃时)。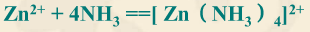
第2题
对于原电池:(一)Zn|zn2+(c1)||Zn2+(c2)|Zn(),下列说法正确的是()。
A.这种电池的电动势必然为零
B.当c1>c2时构成自发电池
C.当c1<c2时构成自发电池
D.当c1≠c2时电池电动势为零
第3题
已知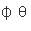 (Zn2+/Zn)=-0.762V,
(Zn2+/Zn)=-0.762V,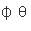 (Cu2+/Cu)=0.342V,[Zri(NH3)4]2+的Ks=2.9×109,[Cu(NH3)4]2+的Ks=2.1×1013。计算下列电池的电动势:
(Cu2+/Cu)=0.342V,[Zri(NH3)4]2+的Ks=2.9×109,[Cu(NH3)4]2+的Ks=2.1×1013。计算下列电池的电动势:
(-)Zn|[Zn(NH3)4]2+(0.100mol·L-1),NH3·H2O(1.00mol·L-1)‖NH3·H2O(1.00mol·L-1),[Cu(NH3)4]2+(0.100mol·L-1)|Cu()
第4题
已知298K时下列电极电势: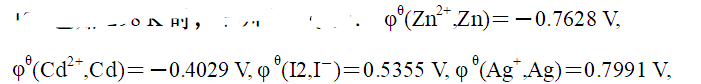 ,下列电池的标准电动势最大的是:
,下列电池的标准电动势最大的是:
(A) Zn(s)|zn2+||cd2+|Cd(s) (B) Zn(s)|zn2+||H+|H2,Pt
(C) Zn(s)|Z2+||I-|I2,Pt (D) Zn(s)|Zn2+||Ag+|Ag(s)
第5题
A.这种电池的电动势必然为零
B.当c1>c2时构成自发电池
C.当c1<c2时构成自发电池
D.当c1≠c2时电池电动势为零
第6题
反应Zn(s)+Hg2Cl2(s)====2Hg(l)+Zn2+(aq)+2Cl-(aq)在25℃下,当各离子浓度均为1.0mol·dm-3时,测得电池电动势为1.03V,当c(Cl-)=0.100mol·dm-3时,电动势为1.21V,此时c(Zn2+)为多少?
第7题
计算下列电池的电动势,说明该电池是原电池还是电解池。
(-)Zn|Zn2+(5×10-4mol·L-1)||

已知:
第8题
反应:Zn(g)+2H+(mol·L-1)====Zn2+(1.0mol·L-1)+H2(100kPa),测得该电池反应的电池电动势为0.46V,求氢电极中溶液的pH。已知(Zn2+/Zn)=-0.76V。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
