 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.电源节能
B.动力节能
C.照明节能
D.政府制定政策
 更多“电气节能的主要途径有()。A.电源节能B.动力节能C.照明节能D.政府制”相关的问题
更多“电气节能的主要途径有()。A.电源节能B.动力节能C.照明节能D.政府制”相关的问题
第1题
测定化合物S的一种酶催化反应速率的实验结果如下表:
时间/min | 0 | 20 | 60 | 100 | 160 |
5的浓度/(mol·L-1) | 1.0 | 0.9 | 0.7 | 0.5 | 0.2 |
试判定在上述浓度范围内的反应级数。
第2题
进行氢氧化钠与乙酸乙酯的反应,实验数据如下表所示,求反应级数与反应速率常数。
时间t(s) | NaOH(mol/L) | CH3COOC2H5(mol/L) |
0 | 0.5638 | 0.3114 |
393 | 0.4866 | 0.2342 |
669 | 0.4467 | 0.1943 |
1010 | 0.4113 | 0.1589 |
1265 | 0.3879 | 0.1354 |
第3题
酶(E)作用在某一底物(S)上生成产物P,现实验测定不同Cs,0时反应的初始速率,数据如下
1.jpg) 已知CE,0=2.80×10-9mol.dm-3,试计算KM和k2。
已知CE,0=2.80×10-9mol.dm-3,试计算KM和k2。
第4题
273℃时,测得反应2NO(g)+Br2(g)→2NOBr(g)在不同的反应物初始浓度下的初始反应速率如下表所示:
实验编号 | 初始浓度/mol·dm-3 | 初始速率 | |
NO | Br2 | ||
1 | 0.10 | 0.10 | 12 |
2 | 0.10 | 0.20 | 24 |
3 | 0.10 | 0.30 | 36 |
4 | 0.20 | 0.10 | 48 |
5 | 0.30 | 0.10 | 108 |
试求:(1) 反应级数;(2) 速率常数;(3) 速率方程式。
第5题
实验测得反应2N2O5 4NO2+O2在340K时,N2O5的浓度随时间变化的数据如下表所示,求反应进行到2min时的反应速率。
4NO2+O2在340K时,N2O5的浓度随时间变化的数据如下表所示,求反应进行到2min时的反应速率。
| t/min | 0 | 1 | 2 | 3 | 4 |
| c(N2O2)/mol·L-1 | 0.160 | 0.113 | 0.080 | 0.056 | 0.040 |
第6题
在660 K时,反应2NO+O2=2NO2的有关实验数据如下表所示,求

反应的速率方程及反应级数。
第7题
有一酶催化反应CO2(aq)+H2O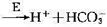 ; 设H2O大大过量,溶液的pH=7. 1,温度为0. 5℃,酶的初始浓度
; 设H2O大大过量,溶液的pH=7. 1,温度为0. 5℃,酶的初始浓度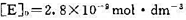 。实验测得反应初速率ro随CO2(g)的初始浓度[CO2]。的变化如下所示:
。实验测得反应初速率ro随CO2(g)的初始浓度[CO2]。的变化如下所示:

试求:(1) Michaelis常数Km及最大反应速率rm; (2)中间配合物的速率常数k2;(3)从速率方程如何理解Km是反应速率为最大反应速率rm的一半时底物的浓度,即r=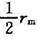 时,KM= [S].
时,KM= [S].
第8题
酶反应动力学的米氏公式为
当cS=Km时,试推导酶反应的级数,此时,利用上式监测转化速率,可测定何类物质?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
