 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“砂浆应具有良好的流动性和保水性。砂浆的流动性是用______表示,砂浆的保水性是用______表示。”相关的问题
更多“砂浆应具有良好的流动性和保水性。砂浆的流动性是用______表示,砂浆的保水性是用______表示。”相关的问题
第1题
(1)一含有Ag2C2O4和CaC2O4沉淀的溶液中,c(Ca2+)=0.10mol·L-1。计算溶液中银离子浓度c(Ag)。
(2)向银电极Ag+/Ag中,加入足量的和Ca2+,反应达平衡后溶液中钙离子浓度c(Ca2+)=0.10mol·L-1。计算此时该电极的电极电势φ(Ag+/Ag)。
此时的银电极,已变为金属(Ag)与两种含有相同阴离子的难溶盐(Ag2C2O4和CaC2O4)及与第二种难溶盐所含有的水合阳离子(Ca2+)组成的电极系统,此类电极称为第三类电极。请根据(Ag+/Ag)计算该电极的标准电极电势,并写出其能斯特方程。试分析第三类电极的特点,预计有何实际应用。
已知:(Ag2C2O4)=1.0×10-11,
(CaC2O4)=2.3×10-9,
(Ag+/Ag)=0.80V
第2题
第4题
已知298.15K时,电极反应:
V,Ag2C2O4的Ksp为3.5×10-11,求电极反应

的标准电极电势
。
第5题
已知298.15K时,电极反应: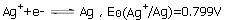 ,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e-
,Ag2C2O4的Ksp为3.5×10-11,求电极反应Ag2C2O2+2e- 2Ag+C2O2-4的标准电极电势
2Ag+C2O2-4的标准电极电势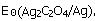 。
。
第6题
10.已知(Ag+/Ag)=0.7996V,
(Ag2CrO4)=1.12×10-12,计算电极反应
的标准电极电势以及当时该电极反应的电势值。
第7题
已知E(Ag+/Ag)=0.7996V,Ksp(Ag2CrO4)=1.12×10-12,计算电极反应
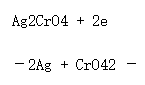 的标准电极电势以及当
的标准电极电势以及当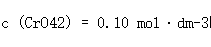 时该电极反应的电势值。
时该电极反应的电势值。
第8题
已知电对Ag++e→Ag的EΘ=+0.799V。Ag2C2O4的溶度积为5.4×10-12。试计算电对Ag2C2O4(s)+2e→2Ag+C2O2-的标准电极电势。
第9题
A.-0.7991V
B.0.7991V
C.-1.60V
D.1.60V

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
