 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.氧化铝坩埚可用于熔融NaOH实验
B.铝与Fe2O3发生反应,反应后固体物质增重
C.氧化铝熔点很高,可作耐火材料
D.明矾用作净水剂,可以除去废水中的铜离子
 答案
答案
 更多“下列关于铝及其化合物的叙述正确的是()”相关的问题
更多“下列关于铝及其化合物的叙述正确的是()”相关的问题
第4题
A.不许使用碱性硫化试剂,因为硫可以和银发生反应
B.银的熔点960℃,不能在火上直接加热
C.不受KOH(NaOH)的侵蚀,在熔融此类物质时仅在接近空气的边缘处略有腐蚀
D.熔融状态的铝、锌等金属盐都能使银坩埚变脆,不可用于熔融硼砂
E.可以用于沉淀物的灼烧和称重
第5题
A.都有H2O生成
B.都有H2生成
C.反应后铝元素主要以[Al(OH)4]-的形式存在
D.反应后铝元素主要以Al3+的形式存在
第6题
阅读下列三段材料,根据要求完成任务。
材料一《普通高中化学课程标准(实验)》关于金属及其化合物的内容标准:根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质,能列举合金材料的重要应用。
材料二某版本高中实验教科书《化学l》“铝的重要化合物”的内容:二、铝的重要化合物
铝是地壳中含量最多的金属元素,但人们发现并制得单质铝却比较晚,这是由于铝很活泼.从铝的化合物中提炼铝单质比较困难。铝的许多化合物在人类的生产和生活中具有重要的作用。
1.氧化铝
我们已经知道,氧化铝难溶于水,熔点很高,也很坚固,因此覆盖在铝制品表面极薄的一层氧化铝就能有效地保护内层金属。氧化铝是冶炼金属铝的原料,也是一种比较好的耐火材料。
它可以用来制造耐火坩埚、耐火管和耐高温的实验仪器等。
氧化铝难溶于水,却能溶于酸或强碱溶液中。它溶于碱时,生成物是偏铝酸盐和水。因此,氧化铝是一种两性氧化物。
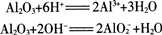
2.氢氧化铝【实验3-7】
在试管里加入l0 mL 0.5 mol/L Al2(S04)3溶液,滴加氨水,生成白色胶状物质。继续酒加氨水.直到不再产生沉淀为止。
反应中得到的白色胶状物质是氢氧化铝[AI(OH)3],它几乎不溶于水,但能凝聚水中的悬浮物.并能吸附色素。在实验室里,常常用铝盐溶液与氨水反应来制取氢氧化铝。
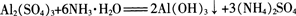
【实验3-8】
取一些上面实验中制得的AI(OH),沉淀,分装在2支试管里,往一支试管里滴加2 mol/L盐酸.往另一支试管里滴加2 mol/L NaOH溶液。边加边振荡,观察现象。
实验证明,AI(OH)3在酸或强碱溶液里都能溶解。这说明它既能与酸起反应,又能与强碱起反应.它是两性氢氧化物。
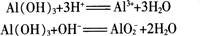
AI(OH)3是医用的胃酸中和剂中的一种,它的碱性不强,不至于对胃壁产生强烈的刺激或腐蚀作用,但却可以与酸反应,使胃液酸度降低,起到中和过多胃酸的作用。
加热时,AI(OH)3分解为氧化铝和水。
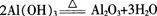
【学与问】
问题:为什么常用氨水与硫酸铝溶液反应制取氢氧化铝,而不用氢氧化钠溶液?
材料三教学对象为高中一年级学生,他们已经学习了必修化学1的“铝单质”“物质的分类”以及“离子反应”等知识。
要求:
(1)回答材料二“学与问”中的问题。
(2)完成“铝的重要化合物’’的教学设计片段,内容包括教学目标、教学方法和教学过程。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
