 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
向0.10mol/L 的HAc溶液中加入少量NaAc固体,电离平衡向 移动(填左或者右),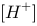 浓度 ,解离度 ,若加入少量HCl,
浓度 ,解离度 ,若加入少量HCl,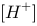 ,解离度 ,若加入较多NaCl固体,解离度 ,pH值 。(以上空格填增大,或者减小)
,解离度 ,若加入较多NaCl固体,解离度 ,pH值 。(以上空格填增大,或者减小)
 更多“向0.10mol/l 的hac溶液中加入少量naac固体,电离平衡向 移动(填左或者右),”相关的问题
更多“向0.10mol/l 的hac溶液中加入少量naac固体,电离平衡向 移动(填左或者右),”相关的问题
第1题
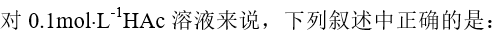
A、加入浓HAc,由于反应物浓度增加,平衡向右移动,HAc的解离度增大
B、用水稀释,HAc的解离度减小
C、加入少量NaOH,HAc的解离平衡向左移动
D、加入少量HCl,HAc的解离度减小
第2题
A、NaOH
B、HCl
C、H2S
D、NH3
第9题
从标准电极电位可以看出,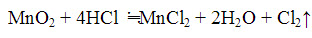 反应是向左进行;但在实验室里,用此反应可制取氯气,对此反应解释应是()
反应是向左进行;但在实验室里,用此反应可制取氯气,对此反应解释应是()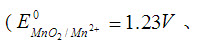
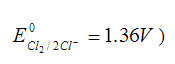 。
。
A. 增加盐酸溶液的用量,可使平衡向右移动
B. 增大盐酸的浓度,可提高二氧化锰电对的电极电位
C. 增大盐酸的浓度,可提高二氧化锰电对的电极电位,同时降低氯电对的电极电位,从而改变化学反应的方向
D. 增大盐酸的浓度,可提高二氧化锰电对的电极电位,同时加热使氯气在水中电离度降低,从而改变化学反应的方向

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
