 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“乙醇(1)-甲苯(2)二元系统的在 T=318 K, p=24.4 kPa下达到汽液平衡。该条件下的汽液平衡表达式为 。(表达式分子分母各置于括号中,角标书写跟在字母后,若有角标先写下标后上标,乘号用…”相关的问题
更多“乙醇(1)-甲苯(2)二元系统的在 T=318 K, p=24.4 kPa下达到汽液平衡。该条件下的汽液平衡表达式为 。(表达式分子分母各置于括号中,角标书写跟在字母后,若有角标先写下标后上标,乘号用…”相关的问题
第1题

第3题
第4题
容积为20dm3的密闭容器中共有2mol的H2O成气液两相平衡。已知:80℃,100℃下水的饱和蒸气压分别为P1=47.343kPa及P2=101.325kPa。25℃水的摩尔蒸发焓△vapHm(298.15K)=44.016kJ·mol-1;水和水蒸气在25~100℃间的平均摩尔定压热容Cp,m(H2O,l)=75.75J·mol-1·K-1及Cp,m(H2O,g)=33.76J·mol-1·K-1。今将系统从80℃的平衡态,加热到100℃的平衡态。求过程的Q,△U,△H及△S。
第5题
容积为20dm3的密闭容器中共有2mol的H2O成气液两相平衡。已知:80℃,100℃下水的饱和蒸气压分别为P1=47.343kPa及P2=101.325kPa。25℃水的摩尔蒸发焓△vapHm(298.15K)=44.016kJ·mol-1;水和水蒸气在25~100℃间的平均摩尔定压热容Cp,m(H2O,l)=75.75J·mol-1·K-1及Cp,m(H2O,g)=33.76J·mol-1·K-1。今将系统从80℃的平衡态,加热到100℃的平衡态。求过程的Q,W,△U,△H及△S。
第6题

若将压力从100kPa提高到50000kPa,问:
(1)若各气体仍作为理想气体处理,其标准平衡常数有无变化?
(2)若各气体的逸度因子分别为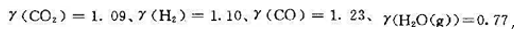 ,则平衡应向何方移动?
,则平衡应向何方移动?
第7题
密闭容器中反应 2NO(g)+O2(g)![]() 2NO2(g)在1500K条件下达到平衡。若始态p(NO)=150kPa,p(O2)=450kPa,p(NO2)=0;平衡时p(NO2)=25kPa。试计算平衡时p(NO),p(O2)的分压及平衡常数KΘ。
2NO2(g)在1500K条件下达到平衡。若始态p(NO)=150kPa,p(O2)=450kPa,p(NO2)=0;平衡时p(NO2)=25kPa。试计算平衡时p(NO),p(O2)的分压及平衡常数KΘ。
第8题
已知甲苯、苯在90℃下纯液体的饱和蒸气压分别为54.22kPa和136.12kPa。两者可形成理想液态混合物。取200.0g甲苯和200.0g苯置于带活塞的导热容器中,始态为一定压力下90℃的液态混合物。在恒温90℃下逐渐降低压力,问:(1)压力降到多少时,开始产生气相,此气相的组成如何?(2)压力降到多少时,液相开始消失,最后一滴液相的组成如何?(3)压力为92.00kPa时,系统内气一液两相平衡,两相的组成如何?两相的物质的量各为多少?
第9题
1mol理想气体在T=300K下,从始态100kPa经下列各过程,求Q,△S及△Siso。(1)可逆膨胀到末态压力50kPa;(2)反抗恒定外压50kPa不可逆膨胀至平衡态;(3)向真空自由膨胀至原体积的2倍。

第10题
1mol理想气体在T=300K下,从始态100kPa经下列各过程,求Q,△S及△Siso。(1)可逆膨胀到末态压力50kPa;(2)反抗恒定外压50kPa不可逆膨胀至平衡态;(3)向真空自由膨胀至原体积的2倍。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
