 更多“理想气体混合物中某气体的分压越大,该气体化学势越大。”相关的问题
更多“理想气体混合物中某气体的分压越大,该气体化学势越大。”相关的问题
第1题
理想气体反应在一定温度下达到平衡。若使体系总体积不变,加入一种惰性气体组分后,各气体分压( )、各气体的化学势( )、平衡常数( )。
A、不变、不变、变化
B、不变、不变、不变
C、变化、变化、不变
点击查看答案
第2题
设A(g)和B(g)两种组分组成的混合理想气体,温度为T,总压力为p,A(g)的摩尔分数为yA。试写出A(g)的化学势表达式,并指出化学势的标准态( )。
点击查看答案
第3题
[图]A、逸度 f = pθ的实际气体的化学势B、压力 p = pθ的...
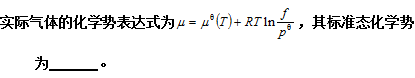
A、逸度 f = pθ的实际气体的化学势
B、压力 p = pθ的实际气体的化学势
C、压力 p = pθ的实际气体的化学势
D、逸度 f = pθ的理想气体的化学势
点击查看答案
第4题
实际气体的化学势表达式,其中标准态化学势为 A. 逸度f = pθ的实际气体的化学势 B. 压力p = pθ的实际气体的化学势 C. 压力p = pθ的实际气体的化学势 D. 逸度f = pθ的理想气体的化学势
点击查看答案
第5题
由分压定律可导出理想气体反应Kθ与Kx的关系.能否用化学势表达式直接导出Kx?此时的标准态是什么?此时的标准态化学势与惯用的气体标准态(pθ)化学势之间的关系如何?
点击查看答案
第6题
以下说法对吗?错的请改正,正确的说明原因。 (1) 温度、压力没有偏摩尔量。 (2) 恒温恒压下,纯物质的量越多,其化学势越大。 (3) 自然界中没有真正的理想气体和理想溶液,因为两者都是分子间无作用力的模型。 (4) 凝固点降低常数与溶剂、溶质的种类都有关。 (5) 非理想溶液中溶剂和溶质的标准态与理想溶液相同。
点击查看答案
第7题
以下说法对吗?错的请改正。 (1) 温度、压力没有偏摩尔量。 (2) 恒温恒压下,纯物质的量越多,其化学势越大。 (3) 自然界中没有真正的理想气体和理想溶液,因为两者都是分子间无作用力的模型。 (4) 凝固点降低常数与溶剂、溶质的种类都有关。 (5) 非理想溶液中溶剂和溶质的标准态与理想溶液相同。
点击查看答案
第8题
以下说法对吗?为什么? (1) 温度、压力没有偏摩尔量。 ( ) (2) 恒温恒压下,纯物质的量越多,其化学势越大。 ( ) (3) 自然界中没有真正的理想气体和理想溶液,因为两者都是分子间无作用力的模型。( ) (4) 稀溶液的沸点一定比纯溶剂的沸点高。( ) (5) 凝固点降低常数只与溶剂的种类有关,而与溶质的性质无关。( )
点击查看答案
 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 更多“理想气体混合物中某气体的分压越大,该气体化学势越大。”相关的问题
更多“理想气体混合物中某气体的分压越大,该气体化学势越大。”相关的问题
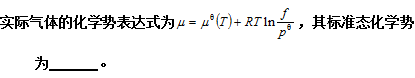

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
