 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下述电池的电动势为0.893V,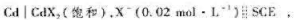
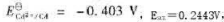 计算
计算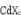 的溶度积常数。
的溶度积常数。
 更多“下述电池的电动势为0.893V,计算的溶度积常数。”相关的问题
更多“下述电池的电动势为0.893V,计算的溶度积常数。”相关的问题
第2题
下列电池的电动势为0.048V,计算AgI的溶度积常数![]() =?
=?
![]() (Ag[+/Ag)=+0.799V]
(Ag[+/Ag)=+0.799V]
(-)Ag,AgI(s)|NaI(0.020mol·L-1)||H+(a=1mol·L-1)|H2(101.325kPa)|Pt(+)。
第3题
为了测定的溶度积,设计了下列原电池:![]()
在25℃时测得电池电动势EΘ=0.22V,求PbSO4溶度积常数![]()
第4题
下述电池的电动势为0.972V(25℃)Cd|CdX2,X-(0.0200mol·dm-3)||SCE已知![]() ,忽略液接电位的影响,计算25℃时CdX2的
,忽略液接电位的影响,计算25℃时CdX2的![]() 。
。
第5题
下述电池的电动势为0.411V:
Mg2+离子选择电极|Mg2+(a=1.77×10-3mol·L-1)‖饱和甘汞电极当此已知镁活度的溶液由一未知液取代后,电动势为0.439V。未知液中的pMg为何值?
第6题
计算298K时下述电池的电动势E。
Pb(s)|PbCl2(s)|HCl(0.01mol·kg-1)|H2(10kPa)|Pt
已知![]() =-0.126V,该温度下PbCl2(s)在水中饱和溶液的浓度为0.039mol·kg-1(用Debye-Huckel极限公式求活度因子后再计算电动势)。
=-0.126V,该温度下PbCl2(s)在水中饱和溶液的浓度为0.039mol·kg-1(用Debye-Huckel极限公式求活度因子后再计算电动势)。
第7题
下列电池的电动势为0.981V。Zn|Zn2+(5.0×10-3mol/L),NH3(0.12mol/L)![]() SHE计算下述反应的平衡常数K(25℃时)。
SHE计算下述反应的平衡常数K(25℃时)。![]()
第8题
下列电池的电动势为0.981V。
(—)Zn|Zn2+(5.0×10-3mol/L),NH3(0.12mol/L)![]() SHE(+)
SHE(+)
计算下述反应在25℃时的平衡常数K。{Zn2++4NH3====[Zn(NH3)4]2+,E=-0.763V}
第10题
在298K时,下述电池的电动势E=0.1519V:
Ag(s)|AgI(s)|HI(a=1)|![]() |Pt
|Pt
并已知下列物质的标准摩尔生成焓:
| 物 质 | AgI(s) | Ag+ | I- |
 | -62.38 | 105.89 | -55.94 |
试求:![]()


 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
