 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。
(I)写出通过晶胞中心的点对称元素。
(2)根据Na+和Cl-的离子半径值,了解在这结构中负离子是否接触?这种结构的稳定性如何?
(3)试计算NaCl晶体的密度D。
(4)将图C.17.1晶胞中顶角上的Na+和中心的Cl-除去,将Na+换成Nb2+,Cl-换得O2-即得NbO晶胞,试画出NbO的晶胞和其中原子簇的结构;已知晶跑参数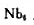 =421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
=421pm,计算晶体的密度i写出通过晶胞中心点的点对称元素和点群(Nb的相对原子质量为92.91);计算Nb2+的离子半径。
(5)将图C.17.1晶胞中面心和体心的原子除去,顶角上的Na+换成U6+,棱上的Cl-换成O2-,得UO3的晶体结构,立方晶胞参数a=415.6pm。试画出UO3晶胞的结构;写出通过晶胞中心点的点对称元素和点群;计算晶体的密度,计算U6+的离子半径(U的相对原子质量为238.0);画出由处在12条棱上的02-组成的立方八面体的图形;计算该多面体的自由孔径。
 更多“已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。(I)写出通过晶”相关的问题
更多“已知NaCl的晶体结构如图C.17.1所示,它属于立方晶系,Oh点群。晶胞参数=564.0pm。(I)写出通过晶”相关的问题
第1题
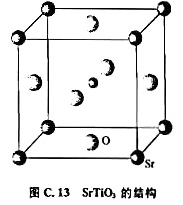
(1)按计算键价公式和查得的计算键价的参数,计算Ti-O键和Sr-O键的键价,计算结构中Ti4+和Sr2+的键价和。
(2)若将O2-和Sr2+一起进行密堆积,这种堆积属于什么型式?Ti4+填入到什么样的空隙中?这种空隙由什么原子组成?
(3)已知CaTiO3立方晶胞参数a=394pm,计算晶体中Ca2+和Ti4+的键价和,用此结果评述文献中报道“CaTiO3的结构实际上是正交晶系晶体,Ca2+和Ti4+的配位情况不像图C.13那样规整,只有当温度升高到900℃,才真正变为立方晶系晶体”。
(4)已知BaTiO3立方晶胞参数a=401.2pm,计算Ba2+和Ti4+的键价和。说明BaTiO3成为重要的铁电材料的内部结构依据。
第2题
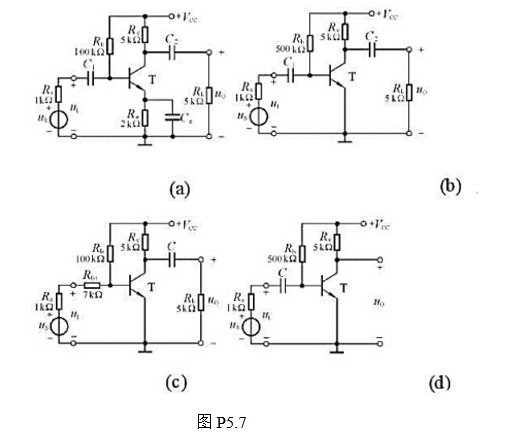
(1)低频特性最差即下限频率最高的电路是().
(2)低频特性最好即下限频率最低的电路是().
(3)高频特性最差即上限频率最低的电路是().
第4题
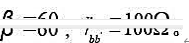
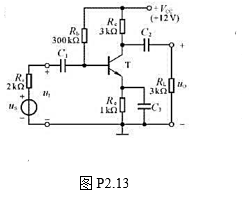
(1)求解Q点、Au、Ri,和R0;
(2)设Us=10mV(有效值),问Ui=若C3开路,则Ui=?,U0=?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
