 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
以K2Cr2O2标准溶液滴定Fe2+,计算25℃时反应的平衡常数;若化学计量点时Fe3+的浓度为0.05000mol·L-1,要使反应定量进行,所箭H+的最低浓度为多少?(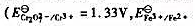
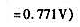 )
)
 更多“以K2Cr2O2标准溶液滴定Fe2+,计算25℃时反应的平衡常数;若化学计量点时Fe”相关的问题
更多“以K2Cr2O2标准溶液滴定Fe2+,计算25℃时反应的平衡常数;若化学计量点时Fe”相关的问题
第1题
计算pH=10.0,在总浓度为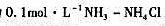 缓冲溶液中,Ag+/Ag电对的条件电势。忽略离子强度及形成
缓冲溶液中,Ag+/Ag电对的条件电势。忽略离子强度及形成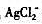 络合物的影响(Ag-NH3络合物的
络合物的影响(Ag-NH3络合物的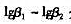 分别为3. 24,7.05;
分别为3. 24,7.05; )
)
请帮忙给出正确答案和分析,谢谢!
第2题
以 溶液滴定20.00mLO.0500mol·L-1的12溶液(含Kllmol·L-1)。计算滴定分数为0.50,1.00及1.50时体系的电势各为多少?
溶液滴定20.00mLO.0500mol·L-1的12溶液(含Kllmol·L-1)。计算滴定分数为0.50,1.00及1.50时体系的电势各为多少?
请帮忙给出正确答案和分析,谢谢!
第3题
第4题
已知I2在水中的溶解度为0.00133mol·L-1,求以0. 1000mol. L-1Ce4+滴定50.00mL等浓度的I-时,固体I2刚刚开始出现沉淀时,消耗的Ce4+为多少毫升?( 的K=708)
的K=708)
请帮忙给出正确答案和分析,谢谢!

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
