 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
测定某试样中锰和钒的含量,称取试样1.000g,溶解后,还原为Mn2+和V02+,用0.02000mol. L-1KMnO4标准溶液滴定,用去2.50mL。加入焦磷酸(使Mn3+形成稳定的焦磷酸络合物)继续用上述KMnO4标准溶液滴定生成的Mn2+和原有的Mn2+到Mn3+,用去4.00mL。计算试样中锰和钒的质量分数。
 更多“测定某试样中锰和钒的含量,称取试样1.000g,溶解后,还原为Mn2+和V02+,用0.02000mo”相关的问题
更多“测定某试样中锰和钒的含量,称取试样1.000g,溶解后,还原为Mn2+和V02+,用0.02000mo”相关的问题
第1题
一自动缓冲装置上的铬板的厚度可以用下面方法测定。把30cm2的缓冲装置的铬板溶于酸中并用
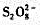 把Cr3+氧化为
把Cr3+氧化为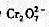 ,煮沸,除去多余的
,煮沸,除去多余的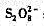 ;加入
;加入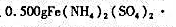 ,
,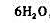 把
把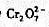 还原为Cr3+,多余的Fe2+被0.00389mol·L-1的K2Cr2O7返滴定,达到终点时共用去K2Cr2O7,18.29mL。试确定铬板的平均厚度。已知Cr的密度为7.20g/cm3。
还原为Cr3+,多余的Fe2+被0.00389mol·L-1的K2Cr2O7返滴定,达到终点时共用去K2Cr2O7,18.29mL。试确定铬板的平均厚度。已知Cr的密度为7.20g/cm3。
第2题
浓度的过氧乙酸。准确称取0.5030g过氧乙酸试样,置于预先盛有40mL水,5mL ,3mol·L-1H2S04溶液和2-3滴1mol·L-1MnSO4溶液并已冷却至5℃的碘量瓶中摇匀,用0.0237mol·L-1KMnO4标准溶液滴定至溶液呈浅粉红色(30s不褪色) ,消耗12.5mL;随即加入10mL 20% KI溶液和2 ~3滴(NH4)2MoO4溶液(起催化作用并减轻溶液的颜色),轻轻摇匀,加塞,在暗处放置5~10min,用0.102mol·L-1Na2S2O3标准溶液滴定,接近终点时加入3mL,0. 5%淀粉指示剂,继续滴定至蓝色消失,消耗Na2S2O323.6mL。写出与滴定有关的化学反应方程式并计算过氧乙酸的质量分数(M=76. 05g·mol-1)
第3题
用间接碘量法测定制时,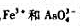 都能氧化I+而干扰铜的测定,加入0.005mol·L-1NH4HF2即能消除
都能氧化I+而干扰铜的测定,加入0.005mol·L-1NH4HF2即能消除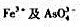 的干扰。试以计算说明之。
的干扰。试以计算说明之。
第4题
第5题
少量的碘化物可利用“化学放大”反应进行测定,其步骤如下:在中性或弱酸性介质中先加Br2然后加入过量的KI,用CCL4萃取生成的I2(萃取率E=100% )。分去水相后,用肼(即联氨)的水溶液将I2反萃至水相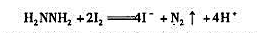 ,再用过量的Br2氧化,除去剩余的Br2后加入过量KI,酸化,以淀粉作指示剂,用Na2S2O3标准溶液滴定,求得I2的含量。
,再用过量的Br2氧化,除去剩余的Br2后加入过量KI,酸化,以淀粉作指示剂,用Na2S2O3标准溶液滴定,求得I2的含量。
a.写出上述过程的有关反应方程式;
b.根据有关的反应计量关系,说明经上述步骤后,试样中1mol的I可消耗几摩尔Na2S2O3相当于“放大”到多少倍?
c.若在测定时,准确移取含KI的试液25.00mL。终点时耗用0.100mol·1L-1Na2S2O3溶液20.06mL,试计算试液中KI的浓度(g.L-1)。已知MKI=166g·mol-1
第6题
在碱性条件下,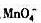 可以用作分析Mn2+的滴定剂,待测组分和滴定剂的产物均为MnO2。在一锰的矿物分析中,0.5165g试样被溶解,然后Mn被还原为Mn2+,碱化该溶液并用0.03358mol·L-1的KMnO4滴定该溶液,达到滴定终点时需要34.88mLKM4计算矿物中Mn的含量。
可以用作分析Mn2+的滴定剂,待测组分和滴定剂的产物均为MnO2。在一锰的矿物分析中,0.5165g试样被溶解,然后Mn被还原为Mn2+,碱化该溶液并用0.03358mol·L-1的KMnO4滴定该溶液,达到滴定终点时需要34.88mLKM4计算矿物中Mn的含量。
第7题
根据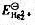 和Hg2Cl2的Kap ,计算
和Hg2Cl2的Kap ,计算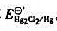 如溶液中Cl-浓度为0.010mol·L-1,Hg2Cl2/Hg电对的电势为多少?
如溶液中Cl-浓度为0.010mol·L-1,Hg2Cl2/Hg电对的电势为多少?
第8题
分别计算0.100mol·L-1KMnO4和0.100mol·L-1K2Cr2O2在H+浓度为1.0mol·L-1介质中,还原一半时的电势。计算结果说明什么?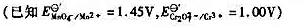
第9题
红色粉末状固体Pb3O4的化学式可写成2PbO、PbO2,可采用碘量法和络合滴定法连续测定其组成。请依下列实验方法写出nPbO2 和nPbO的计算公式。准确称取0.0400~0.0500g干燥好的Pb3O4固体,置于250mL锥形瓶中。加入HAc-NaAc(1:1) 10mL,再加入0.2mol/L KI溶液1~2mL充分溶解,使溶液呈透明橙红色。加0.5mL 2%淀粉溶液,用0.01mol/L Na2S2O3标准溶液滴定使溶液由蓝色刚好褪去为止,记下所用去的Na2S2O3;标准溶液的体积为 。再加入二甲酚橙3~4滴,用0.01mol/LEDTA标准溶液滴定溶液由紫红色变为亮黄色时,即为终点。记下所消耗的EDTA溶液的体积为VEDTA。
第10题
空气中CO的浓度可以通过下面方法测定:让已知体积的空气通过一根充有I2O5的管子,生成CO2和I2,把I2用蒸馏的方法从试管中取出并收集到一个含有过量KI溶液的锥形瓶中形成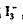 ,然后用Na2S2O3标准溶液滴定这些
,然后用Na2S2O3标准溶液滴定这些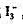 。在一次分析中,4.79L的空气试样按上述方法处理,达到滴定终点时共用去7.17mL0.00329mol·L-1的Na2S2O3溶液。如果空气的密度是1.23x10-3g/mL,试计算空气中CO的含量(用μg.g-1表示)。
。在一次分析中,4.79L的空气试样按上述方法处理,达到滴定终点时共用去7.17mL0.00329mol·L-1的Na2S2O3溶液。如果空气的密度是1.23x10-3g/mL,试计算空气中CO的含量(用μg.g-1表示)。

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
