 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
称取含KBr和KI的混合试样1.000g,溶解并定容至200mL后,作如下测定:
(1)移取50.00mL试液,在近中性条件下,以溴水充分处理,此时I-转变为[IO3]-。将溴驱尽,加入过量KI溶液,酸化,生成的I-采用淀粉指示剂,以0.1000mol/L的Na2S2O3溶液滴定至终点时,消耗30.00mL。
(2)另取50.00mL试液,用H2SO4酸化,加入足量K2Cr2O7溶液处理,将生成的I2和Br2蒸馏并收集在含有过量KI的弱酸性溶液中,待反应完成后,以0.1000mol/LNa2S2O3溶液滴定其中的I2至终点时,消耗15.00mL。
计算混合试样中KI和KBr的质量分数。[Mr(KI)=166.0,Mr(KBr)=119.0]
 更多“称取含KBr和KI的混合试样1.000g,溶解并定容至200mL后,作如下测定:(1)移取50.00mL试液,在近中性”相关的问题
更多“称取含KBr和KI的混合试样1.000g,溶解并定容至200mL后,作如下测定:(1)移取50.00mL试液,在近中性”相关的问题
第1题
少量的碘化物可利用“化学放大”反应进行测定,其步骤如下:在中性或弱酸性介质中先加Br2,然后加入过量的KI,用CCl4萃取生成的I2(苯取率E=100%)。分去水相后,用肼(即联氨)的水溶液将I2反萃至水相: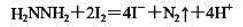 。
。
再用过量的Br2氧化,除去剩余的Br2后加入过量KI,酸化,以淀粉作指示剂,用Na2S2O3标准溶液滴定,求得I-的含量。
a.写出上述过程的有关反应方程式;
b.根据有关的反应计量关系,说明经上述步骤后,试样中1mol的I-可消耗几摩尔Na2S2O3?相当于“放大”到多少倍?
c.若在测定时,准确移取含KI的试液25.00mL,终点时耗用0.100mol?L-1Na2S2O3溶液20.06mL,试计算试液中KI的浓度(g?L-1)。已知MKI=166g?mol-1。
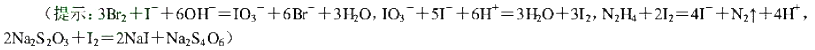
请帮忙给出正确答案和分析,谢谢!
第2题
已知在1mol?L-1H2SO4介质中,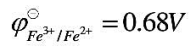 ,1,10-邻二氮菲与Fe3+、Fe2+均能形成配位化合物,加入1,10-邻二氮菲后,体系的条件电势变为1.06V。试问Fe3+与Fe2+和1,10-邻二氮菲形成的配位化合物中,哪一种更稳定?
,1,10-邻二氮菲与Fe3+、Fe2+均能形成配位化合物,加入1,10-邻二氮菲后,体系的条件电势变为1.06V。试问Fe3+与Fe2+和1,10-邻二氮菲形成的配位化合物中,哪一种更稳定?
请帮忙给出正确答案和分析,谢谢!

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
