 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
双环戊烯单分子气相热分解反应,在483 K时的速率常数k(483 K)=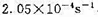 ,在545K时的速率常数k(545 K)=
,在545K时的速率常数k(545 K)=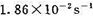 。已知
。已知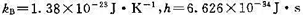 .试计算:(1)反应的活化能
.试计算:(1)反应的活化能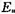 ;(2)反应在500K时的活化焓
;(2)反应在500K时的活化焓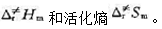
 更多“双环戊烯单分子气相热分解反应,在483 K时的速率常数k(483 K)= ,在545K时的速率常数k(545 K)= 。”相关的问题
更多“双环戊烯单分子气相热分解反应,在483 K时的速率常数k(483 K)= ,在545K时的速率常数k(545 K)= 。”相关的问题
第1题
在恒容下,温度每增加10 K时,
(1)计算碰撞频率增加的百分数;
(2)计算碰撞时在分子连心线上的相对平动能超过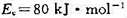 的活化分子对的增加百分数;
的活化分子对的增加百分数;
(3)由上述结果可得出什么结论?
请帮忙给出正确答案和分析,谢谢!
第2题
丁二烯气相二聚反应,反应速率常数k为
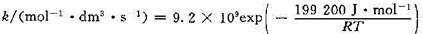
(1)用过渡态理论计算该反应在600 K时的指前因子,已知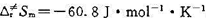 。
。
(2)若有效碰撞直径d=0.5nm,用简单的碰撞理论计算该反应的指前因子;
(3)通过计算讨论概率因子P与活化熵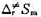 的关系。
的关系。
请帮忙给出正确答案和分析,谢谢!
第3题
O3的光化学分解反应历程如下:
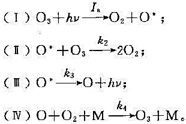
设单位时间、单位体积中吸收光为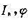 为过程(1 )的量子产率,
为过程(1 )的量子产率,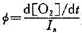 为总反应的量子产率。
为总反应的量子产率。
(1)试证明 (2)若以250.7 nm的光照射时,
(2)若以250.7 nm的光照射时,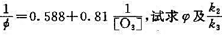 的值。
的值。
请帮忙给出正确答案和分析,谢谢!
第4题
298 K时,反应N2O4(g)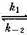 2NO2(g)的速率常数
2NO2(g)的速率常数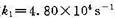 ,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为
,已知N2O4(g)和NO2(g)的标准摩尔生成Gibbs自由能分别为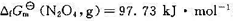 和
和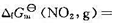 51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
51.25 kJ·mol-1。请计算:(1)在298 K时,N2O4(g)的初始压力为100 kPa,NO2(g)的平衡分压;(2)该反应的弛豫时间r。
请帮忙给出正确答案和分析,谢谢!

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
