 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)


某一溶液中含KCI,KBr和KI的浓度均为0.1 mol·kg-1.今有该溶液放人带有Pt电极的素烧瓷杯内,再将瓷杯放在一带有Zn(s)电极和大量0.1 mol·kg-1的ZnCl2溶液的较大器皿中,若略去液接电势和极化影响,试求298 K时下列情况所需施加的外电压最少为多少。设活度因子均为1.
(1)析出99%的碘;
(2)析出Br2,至Br-浓度为1×10-4mol·kg-1;
(3)析出Cl2,至CI-浓度为1×10-4mol·kg-1.
 更多“某一溶液中含KCI,KBr和KI的浓度均为0.1 mol·kg-1.今有该溶液放人带有Pt电极的素烧瓷杯内,再”相关的问题
更多“某一溶液中含KCI,KBr和KI的浓度均为0.1 mol·kg-1.今有该溶液放人带有Pt电极的素烧瓷杯内,再”相关的问题
第1题
以Ni(s)为电极、KOH水溶液为电解质的可逆氢、氧燃料电池,在298 K和标准压力下稳定地连续工作,试回答下述问题。
(1)写出该电池的表达式、电极反应和电池反应。
(2)求一个100 W(1 W=3.6kJ·h-1)的电池,每分钟需要供给298 K、100 kPa压力的H2(g) ;的体积。已知该电池反应每消耗1 mol H2(g)时的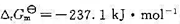 .
.
(3)该电池的电动势为多少?
请帮忙给出正确答案和分析,谢谢!
第3题
在锌电极上析出氢气的Tafel公式为
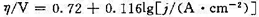
在298K时,用Zn(s)作阴极,惰性物质作阳极,电解浓度为0.1mol·kg-1的ZnSO4溶液,设溶液pH值为7.0,若要使H2(g)不和锌同时析出,应控制什么条件?
请帮忙给出正确答案和分析,谢谢!
第4题
氯碱工业用铁网为阴极,石壘棒为阳极,电解含NaCl的质量分数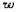 (NaCl)= 0.25的溶液来获得Cl2(g)和NaOH溶液。NaCl溶液不断地加到阳极区,然后经过隔膜进人阴极区。若某电解槽内阻为8×10-4Ω,外加电压为4.5V,电流强度为2000A.每小时从阴极区流出溶液为27.46kg,其中
(NaCl)= 0.25的溶液来获得Cl2(g)和NaOH溶液。NaCl溶液不断地加到阳极区,然后经过隔膜进人阴极区。若某电解槽内阻为8×10-4Ω,外加电压为4.5V,电流强度为2000A.每小时从阴极区流出溶液为27.46kg,其中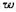 (NaOH) =0.10,
(NaOH) =0.10,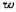 (NaCl)=0.13。已知下述电池的电动势为2.3 V:
(NaCl)=0.13。已知下述电池的电动势为2.3 V:
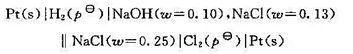
试求:(1)该生产过程的电流效率;(2)该生产过程的能量效率(即生产一定量产品时,理论上所需的电能与实际消耗的电能之比);(3)该电解池中用于克服内阻及用于克服极化的电势降各为多少。
请帮忙给出正确答案和分析,谢谢!

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
