 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
电解质溶液的浓度和离子所带的电荷对平均活度因子都是有影响的。用Debye-Hickel极限公式计算下列强电解质NaCl、MgCl2和FeCl3在浓度分别为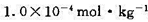 和 5.0×10-4mol·kg-1时的离子平均活度因子。
和 5.0×10-4mol·kg-1时的离子平均活度因子。
 更多“电解质溶液的浓度和离子所带的电荷对平均活度因子都是有影响的。用Debye-Hickel极限公式计算下”相关的问题
更多“电解质溶液的浓度和离子所带的电荷对平均活度因子都是有影响的。用Debye-Hickel极限公式计算下”相关的问题
第1题
298 K时,已知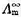 (NaCl)=1.086×10-2S·m2·mol-1,
(NaCl)=1.086×10-2S·m2·mol-1,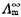 (NaOH)=
(NaOH)=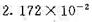
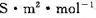 和
和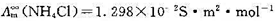 ;
;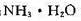 在浓度为 0.1 mol·dm-3时的摩尔电导率
在浓度为 0.1 mol·dm-3时的摩尔电导率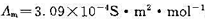 ,浓度为0.01mol·dm-3时的摩尔电导率
,浓度为0.01mol·dm-3时的摩尔电导率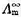 =9.62×10-4S·m2·mol-1。试根据上述数据求
=9.62×10-4S·m2·mol-1。试根据上述数据求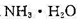 的两种不同浓度溶液的解离度和解离常数。
的两种不同浓度溶液的解离度和解离常数。
请帮忙给出正确答案和分析,谢谢!
第2题
在298 K时,醋酸HAc的解离平衡常数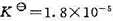 ,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
,试计算在下列不同情况下醋酸在浓度为1.0mol·kg-1时的解离度。(1)设溶液是理想的,活度因子均为1;(2)用Debye-Huckel极限公式计算出γ±的值,然后再计算解离度。设未解离的HAc的活度因子为1.
请帮忙给出正确答案和分析,谢谢!
第4题
在298 K时;用Ag |AgCI为电极,电解KCl的水溶液,通电前溶液中KCl的质量分数为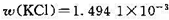 ,通电后在质量为120.99 g的阴极部溶液中
,通电后在质量为120.99 g的阴极部溶液中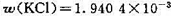 ,串联在电路中的银库仑计中有160.24mg的Ag沉积出来,求K+和CI-的迁移数。
,串联在电路中的银库仑计中有160.24mg的Ag沉积出来,求K+和CI-的迁移数。
请帮忙给出正确答案和分析,谢谢!

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
