 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
CO2(g)与 H2S(g)在高温的反应为 ,今在610 K时将4.4 g的CO2(g)加入体积为2.5 dm3的空瓶中,然后再充入H2S(g)使总压为1000 kPa.达平衡后取样分析,得其中H2O(g)的摩尔分数为0.02。将温度升至620K重复上述实验,达平衡后取样分析,得其中H2O(g)的摩尔分数为0.03。视气体为理想气体,试计算:
,今在610 K时将4.4 g的CO2(g)加入体积为2.5 dm3的空瓶中,然后再充入H2S(g)使总压为1000 kPa.达平衡后取样分析,得其中H2O(g)的摩尔分数为0.02。将温度升至620K重复上述实验,达平衡后取样分析,得其中H2O(g)的摩尔分数为0.03。视气体为理想气体,试计算:
(1) 610K时的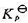 ;
;
(2)610K时的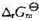 ;
;
(3)反应的标准摩尔焓变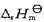 (设其不随温度而变);
(设其不随温度而变);
(4)610K时,往该体积的瓶中充人不参与反应的气体,直至压力加倍,则COS(g)的产量有何变化。若充入不参与反应的气体,保持压力不变,而使体积加倍,COS(g)的产量又有何变化。
 更多“CO2(g)与 H2S(g)在高温的反应为 ,今在610 K时将4.4 g的CO2(g)加入体积为2.5 dm3的空瓶中,”相关的问题
更多“CO2(g)与 H2S(g)在高温的反应为 ,今在610 K时将4.4 g的CO2(g)加入体积为2.5 dm3的空瓶中,”相关的问题
第1题
从NH3(g)制备HNO3的一种工业方法是将NH3(g)与空气的混合物通过高温下的金属Pt催化剂,主要反应为 。计算1 073 K时的标准平衡常数。设反应的
。计算1 073 K时的标准平衡常数。设反应的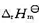 不随温度而改变,所需热力学数据从附录查阅。
不随温度而改变,所需热力学数据从附录查阅。
请帮忙给出正确答案和分析,谢谢!
第3题
(1) 由甲醇可以通过脱氢反应制备甲醛,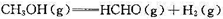 ,试利用
,试利用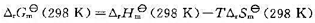 一式,近似估算反应的转折温度,估算973 K时的
一式,近似估算反应的转折温度,估算973 K时的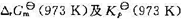 ;
;
(2)电解水是得到纯氢的重要来源之一,能否用水的热分解反应制备氢气?
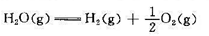
请估算反应的转折温度。所需数据请查阅附录。
请帮忙给出正确答案和分析,谢谢!
第4题
在298 K时,NH4HS(s)在一真空瓶中的分解反应为
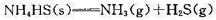
(1)达平衡后,测得总压为66.66 kPa,计算标准平衡常数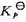 ,设气体为理想气体;
,设气体为理想气体;
(2)若瓶中已有NH3(g) ,其压力为40. 00 kPa,计算这时瓶中的总压。
请帮忙给出正确答案和分析,谢谢!

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
