 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.相同物质的量浓度溶液的pH大小比较:Na2B>NaA>NaHB
B.NaHB溶液中部分微粒浓度的大小比较:c(Na+)>c(HB-)>c(H2B)>c(B2-)
C.将amol•L-1HA溶液与amol•L-1的NaA溶液等体积混合,混合液中的c(Na+)>c(A-)
D.向Na2B溶液中加入足量的HA溶液,发生反应的离子方程式为:B2-+2HA=2A-+H2B
 更多“已知25℃时有关弱酸的电离常数如表所示:则下列说法中正确的是()。”相关的问题
更多“已知25℃时有关弱酸的电离常数如表所示:则下列说法中正确的是()。”相关的问题
第2题
A.25℃时,0.lmol•L-1 HF溶液中pH=l
B.Ksp(CaF2)随温度和浓度的变化而变化
C.该体系中没有沉淀产生
D.该体系中HF与CaC12反应产生沉淀
第3题
A.一定条件下 pH值越大,溶液的酸性越强
B.用pH值表示任何溶液的酸碱性都很方便
C.强酸溶液的pH值一定很小
D.pH值相同的强酸与弱酸中,c(H+)物质的量浓度相同
第4题
A.溶液pH值等于5
B.平衡时酸电离产生的[H+]约为水电离产生的[H+]的10000倍
C.若升高温度,溶液pH值增大
D.若用等体积等物质的量浓度的NaOH溶液与之反应,所得溶液的pH值大于7
第5题
A.常温下,向醋酸溶液中加入少量水,溶液中c(H+)将增大
B.常温下,pH相同的NaOH溶液和Ba(OH)2溶液中,水的电离程度相同
C.向 NaHCO3溶液中加入少量澄清石灰水,所得溶液的pH不变
D.中和等体积、等物质的量浓度的盐酸和醋酸,盐酸所需氢氧化钠多于醋酸
第6题
已知一定温度下的弱电解质的稀溶液,当加水稀释使物质的量浓度变为原来的 1/m时,其电离度将增大到原溶液电离度的.jpg) 倍。现有pH=2的某一元弱酸溶液10mL,加水至1L后,溶液的pH是()。
倍。现有pH=2的某一元弱酸溶液10mL,加水至1L后,溶液的pH是()。
A.等于4
B.在3~4之间
C.等于3
D.在2~3之间
第7题
A.HX、HY都是弱酸,且HX的酸性比HY的弱
B.相同温度下,电离常数K(HX):a>b
C.常温下,由水电离出的c(H+)·c(OH-):a<b
D.lg=3,若同时微热两种溶液,则减小
第8题
A.两种溶液①0.1mol/LHA溶液②0.3mol/LHA溶液与0.1mol/LNaOH溶液等体积混合的混合液;其中c(H+):①<②
B.等物质的量浓度的HA溶液与NaB溶液等体积混合:2c(Na+)=c(A-)+c(B-)+c(HA)+c(HB)
C.pH=9的三种溶液①NaB②NH3·H2O③NaOH,由水电离出的c(OH-):①>②>③
D.物质的量浓度相等的NaA与KB两种溶液中:c(Na+)-c(A-)>c(K+)-c(B-)
第9题
A.当pH=3时,溶液中c(HC2)<c(C2)=c(H2C2O4)
B.pH由3增大到5.3的过程中,水的电离程度逐渐减小
C.常温下,Ka2=10-5.3
D.常温下随着pH的增大:c2(HC2)/[c(H2C2O4)·c(C2)]的值先增大后减小
第10题
下列说法是否正确?若不正确,则予以更正: (1)根据
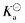 =cα2,弱电解质溶液的浓度越小,则解离度越大,因此,对弱酸来说,溶液越稀,酸性越强(即pH越小)。 (2)在相同浓度的一元酸溶液中,H+离子浓度都相等,因为中和同体积同浓度的醋酸或盐酸,所需的碱是等物质的量的。
=cα2,弱电解质溶液的浓度越小,则解离度越大,因此,对弱酸来说,溶液越稀,酸性越强(即pH越小)。 (2)在相同浓度的一元酸溶液中,H+离子浓度都相等,因为中和同体积同浓度的醋酸或盐酸,所需的碱是等物质的量的。
第11题
A.在稀溶液中: ,则含1mol HClO的稀溶液和含1 mol KOH的稀溶液完全反应放出的热量等于57.3 kJ
B.25℃时,pH=5的醋酸溶液与pH=5的氯化铵溶液中由水电离出的H + 浓度相等
C.10 mL 0.1 mol/L醋酸溶液中加入等物质的量的氢氧化钠后,溶液中离子浓度由大到小的顺序是:
D.向只有 四种离子的某碱性溶液中通入适量二氧化碳,则有:

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
