 重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
重要提示:
请勿将账号共享给其他人使用,违者账号将被封禁!
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.(1)金属铁是由(填原子、分子或 离子,下同)构成的,硫酸铜是由构成的
B.①当a=时,该微粒是原子
C.②当a=8时,该微粒是(填原子、阳离子或 阴离子),其符号为
D.(3)氯化氢是一种无色有刺激性气味的气体,走进实验室就闻到了这种气味。从分子的角度解释这种现象
 更多“回答下列问题()”相关的问题
更多“回答下列问题()”相关的问题
第1题
(1)所标各部件中由金属材料制成的是()(填字母),属于有机合成材料的有()(任选一种部件填字母)。
(2)生铁和钢都是铁的合金,其性能不同的原因是()。
(3)金属矿物储量有限,不可再生。保护金属资源的有效途径,除了防止金属锈蚀外,还有()(写一条即可)。
(4)将一定量的铝、铜粉末混合物加入硝酸银溶液中,充分反应后过滤,滤液为蓝色。则滤渣中一定含有()(填化学式),滤液中溶质的组成可能是()或()(填化学式)。
第2题
右图所示是液态二氧化碳灭火器,请回答下列问题。
(1)图中所标物质中属于金属材料的是()(只写一种),属于有机材料的是________________(只写一种)。
(2)加压在小钢瓶中液态二氧化碳喷出后能灭火。其原理是___________和______________。
(3)在钢瓶表而涂油漆的作用是___________________。
(4)比较铁和铜的金属活动性强弱可采用的方法。

第3题
金属在人类生活和生产中应用十分广泛,下列是关于金属的三组实验,请回答下列问题。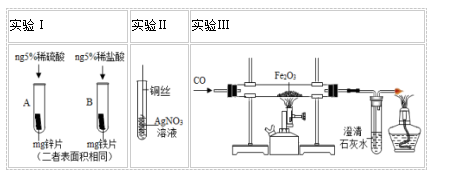 (1)实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为该实验设计不够合理,理由是()。
(1)实验Ⅰ中以“金属表面产生气泡的快慢”为标准来判断锌、铁的活动性强弱,有同学认为该实验设计不够合理,理由是()。
(2)写出实验Ⅱ中C试管内反应的化学方程式()。
(3)实验Ⅲ为实验室模拟炼铁的装置图。
①加热Fe2O3之前要先通一会CO,目的是()。
②装置末加酒精灯装置的目的是()。
第4题
(1)电车外壳的钢铁部分喷涂油漆,它不仅美观,还可以有效地防止铁与()等物质接触而生锈。
(2)电车轨道的主要材料是锰钢,它属于铁的合金,其硬度比纯铁()。
(3)为了探究锰、锌、铁三种金属活动性顺序,某同学设计将锰块、锌粒和铁块分别放入质量和质量分数均相同的稀盐酸中进行实验,该同学实验设计中的不足之处是();写出铁与盐酸反应的化学方程式()。
第5题
回答下列问题: (1)在Fe3+的溶液中加入KNCS溶液时出现了血红色,但加入少许铁粉后,血红色立即消失。 (2)在配制的FeSO4溶液中为什么需加一些金属铁? (3)为什么不能在水溶液中由Fe3+盐和KI制得FeI3? (4)当Na2CO3溶液作用于FeCl3溶液时为什么得到的是氢氧化铁,而不是Fe2(CO3)3? (5)变色硅胶含有什么成分?为什么干燥时呈蓝色,吸水后变粉红色? (6)为什么[CoF6]3-为顺磁性,而[Co(CN)6]3-为抗磁性? (7)为什么[Fe(CN)6]3-为低自旋,而[FeF6]3-为高自旋? (8)为什么[Co(H2O)6]3+的稳定性比[Co(NH3)6]3+低得多(用晶体场理论解释)? (9)为什么将FeO溶解在酸化的H2O2溶液中,与此同时会从溶液中放出氧气?
第7题
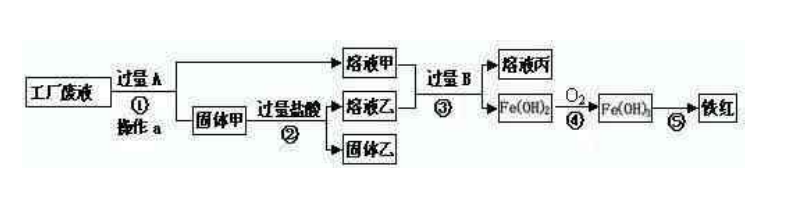
某工厂废液中含有氯化钠.氯化铜和氯化亚铁。某课外小组要从废液中回收铜并得到铁红(主要成分Fe2O3),要求全过程不引入其他金属元素。设计实验方案如下图所示,
回答下列问题。
(1)加入过量A溶解后,再进行操作a时玻璃棒的作用是()。
(2)工厂废液中加入过量A反应的化学方程式为()。
(3)溶液甲中的金属离子是()(写离子符号)。
(4)步骤①②③中所发生的化学反应,其中属于置换反应的是()(填序号)。
(5)铁红是炼铁的主要原料,写出用CO和铁红炼铁的化学方程式()。
第8题
回答下列问题。
(1)FeCl3溶液与Na2CO3溶液作用时为何生成的是氢氧化铁沉淀,而不是碳酸铁沉淀?
(2)Fe3+能腐蚀Cu,而Cu2+又能腐蚀Fe,两者是否有矛盾?试应用有关的电极电势说明之。
(3)实验室使用铂制器皿时,应遵守哪些操作规程,为什么?
(4)铜器在潮湿的空气中放置会慢慢生成一层铜绿。
(5)讨论:Cu(Ⅱ)和Cu(I)相互转化的条件及其化合物的稳定性。
(6)在金属焊接时,为何常用浓ZnCl2溶液处理金属表面?
(7)汞与硝酸反应,当汞过量时为什么生成的是硝酸亚汞?
(8)指出Hg2+和Hg2+2性质上的差异,可用哪些反应来区别它们?
第9题
回答下列问题。
(1)FeCl3溶液与Na2CO3溶液作用时为何生成的是氢氧化铁沉淀,而不是碳酸铁沉淀?
(2)Fe3+能腐蚀Cu,而Cu2+又能腐蚀Fe,两者是否有矛盾?试应用有关的电极电势说明之。
(3)实验室使用铂制器皿时,应遵守哪些操作规程,为什么?
(4)铜器在潮湿的空气中放置会慢慢生成一层铜绿。
(5)讨论:Cu(Ⅱ)和Cu(I)相互转化的条件及其化合物的稳定性。
(6)在金属焊接时,为何常用浓ZnCl2溶液处理金属表面? (7)汞与硝酸反应,当汞过量时为什么生成的是硝酸亚汞? (8)指出Hg2+和Hg2+2性
第10题
根据下图,可以由重晶石(BaSO4)作为原料,制造金属钡及一些钡的化合物。试回答下列问题:
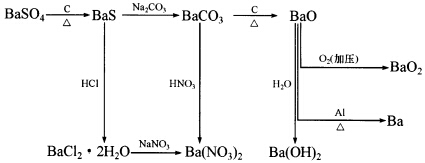 (1)现拟从重晶石制备BaCl2.2H2O。应该采用哪些步骤?写出其化学方程式,并说明完成反应的理由。 (2)为何不能用BaS与硝酸作用直接制备Ba(NO3)2? (3)为何工业上不采用BaCO3直接加热分解方法制备BaO?
(1)现拟从重晶石制备BaCl2.2H2O。应该采用哪些步骤?写出其化学方程式,并说明完成反应的理由。 (2)为何不能用BaS与硝酸作用直接制备Ba(NO3)2? (3)为何工业上不采用BaCO3直接加热分解方法制备BaO?
第11题
回答下列问题:
(1)化学反应的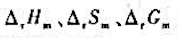 和电池电动势及电极电势值的大小,哪些与化学反应方程式的写法无关?
和电池电动势及电极电势值的大小,哪些与化学反应方程式的写法无关?
(2)为何H2S水溶液不能长期保存?
(3)能否用铁制容器盛放CuSO4溶液?
(4)配制SnCl2溶液时,为防止Sn2+被空气中氧所氧化,通常在溶液中加入少许Sn粒,为什么?
(5)铁溶于过量盐酸或过址稀硝酸,其氧化产物有何不同?
(6)为何金属Ag不能从稀H2SO4或盐酸中置换出H2,,却能从氢碘酸(HI)中置换出H2?

 警告:系统检测到您的账号存在安全风险
警告:系统检测到您的账号存在安全风险
为了保护您的账号安全,请在“上学吧”公众号进行验证,点击“官网服务”-“账号验证”后输入验证码“”完成验证,验证成功后方可继续查看答案!
